1.Medical School, Federal University of Roraima, Boa Vista, Brazília
2.Katedra biotechnológie a biomedicíny, Technická univerzita v Dánsku, Lyngby, Dánsko
3.Katedra fyziky a chémie, Fakulta farmaceutických vied v Ribeirão Preto, Univerzita v São Paule, Ribeirão Preto, Brazília
4.Katedra biotechnológie a biologickej bezpečnosti, Univerzita Eskişehir Osmangazi, Eskişehir, Turecko
5.Katedra biochémie a imunológie, Lekárska fakulta v Ribeirão Preto, Univerzita São Paulo, Ribeirão Preto, Brazília
Včely medonosné možno nájsť po celom svete a plnia kľúčové úlohy opeľovania v rámci svojich prirodzených ekosystémov, ako aj v poľnohospodárstve. Väčšina druhov je zvyčajne učenlivá a väčšina interakcií medzi ľuďmi a včelami je bezproblémová, napriek ich schopnosti vstreknúť do obetí komplexný jed ako obranný mechanizmus. Napriek tomu od náhodného vypustenia afrikanizovaných včiel do Brazílie v roku 1956 a ich následného rozšírenia po celej Amerike počet uštipnutí včiel stúpa. Tieto hybridy včiel sú agresívnejšie a náchylnejšie na útoky, čo predstavuje značnú zdravotnú záťaž pre krajiny, ktoré kolonizovali. Doteraz sa liečba takýchto uštipnutí zvyčajne zameriava na kontrolu potenciálnych alergických reakcií, pretože v súčasnosti neexistujú žiadne špecifické protijedy proti včeliemu jedu. Výskumníci skúmali možnosť vývoja včelích protijedov, ale to bolo komplikované veľmi nízkou imunogenicitou kľúčových včelích toxínov, ktoré nedokázali vyvolať silnú protilátkovú odpoveď u imunizovaných zvierat. So súčasnými špičkovými technológiami, ako je fágový displej, je však popri vzostupe monoklonálnych protilátkových terapeutík dosiahnuteľný vývoj rekombinantného včelieho protijedu a v posledných rokoch boli hlásené sľubné výsledky smerom k tomuto cieľu. Tu sú zhrnuté súčasné poznatky o biológii jedu afrikanizovaných včiel a súčasných možnostiach liečby proti otrave včiel. Okrem toho je prezentovaný a diskutovaný najnovší vývoj v oblasti protijedov novej generácie včiel.
Úvod
Včely sú ekonomicky prospešný hmyz, ktorého existencia siaha do obdobia kriedy počas druhohôr (1). Včely poskytli ľuďom niekoľko produktov, ako je med, včelí vosk, peľ, materská kašička a propolis (2). Opeľujú aj širokú škálu poľnohospodárskych plodín (3). Aj keď sú včely mimoriadne prospešné pre plodiny a ľudí, predstavujú nebezpečenstvo kvôli svojej schopnosti spôsobovať bolestivé a toxické bodnutia (4). Našťastie väčšina včiel medonosných nie je voči ľuďom agresívna a útočia len vtedy, keď sa cítia ohrozené. Avšak kvôli introdukcii afrikanizovanej včely, hybrida s vysoko agresívnym správaním človekom, sa masívne útoky včelieho bodnutia výrazne zvýšili av súčasnosti sú endemické vo väčšine Ameriky (okrem Čile a Kanady) (5). Existujú štandardizované medicínske prístupy na riešenie prípadov, keď sú obete alergické na zložky jedu poštípané včelami, alebo keď miernejšie otravy spôsobí len niekoľko včelích bodnutí. Napriek tomu neexistuje žiadny protijed na liečbu ťažkých jedov včiel. Základným dôvodom je nízka imunogenicita proteínov včelieho jedu (napríklad melittín), ktorá bráni úspešnej imunizácii produkčných zvierat, aby sa dosiahli vysoké titre protilátok v ich plazme, a následne výrazne komplikuje vývoj včelieho protijedu (6). . Na vývoj liečby proti silnému jedu včiel je nevyhnutný návrh účinného protijedu. Tu sú preskúmané súčasné poznatky o biológii včiel, šírení afrikanizovaných hybridov včiel v Amerike a aparáte včelieho jedu a toxínov a poskytuje sa diskusia o súčasnej a ďalšej generácii liečby včelieho jedu.
Druhy včiel, ich správanie a epidemiológia
Včely medonosné (druh Apis) sú spoločenský hmyz, ktorý žije v dobre organizovaných spoločenstvách a je veľmi dôležitý pre významnú časť svetového hospodárstva vďaka kľúčovej úlohe, ktorú plnia ako opeľovače v poľnohospodárstve (7). V poslednom desaťročí sa im však venuje zvýšená pozornosť kvôli inej fyziologickej vlastnosti: ich schopnosti dodať jedovaté bodnutie (8). Druhy včiel, ktoré sú prevažne zodpovedné za ľudské jedy, sú Apis mellifera mellifera (A. m. mellifera) a A. m. ligustica v Európe a A. m. scutellata v Afrike (8).
Včelie žihadlo nie je novým fenoménom. V skutočnosti sa významné vystavenie ľudí včelím bodnutiam datuje pred viac ako 7 000 rokmi, keď ľudia začali spravovať populácie včiel tým, že im poskytli umelé úle, aby umožnili efektívnu úrodu ich medu a vosku alebo na účely opeľovania (9, 10). Napriek značnému šľachtiteľskému úsiliu je potrebné včely úspešne domestikovať a okrem iných vlastností nebolo hlásené zníženie aditívnej genetickej variácie, fixácia alel spojených so znakmi ekonomického významu, zvýšená krotkosť a rozvoj špecifických vlastností plemena ( 11). V skutočnosti sa zdá, že cielené šľachtenie skôr zvýšilo než znížilo genetickú diverzitu (12).
Väčšina komerčných populácií včiel medonosných pochádza z Európy, hoci z evolučného hľadiska pochádzajú z Afriky a do Európy sa dostali prostredníctvom dvoch nezávislých migračných udalostí (13). V 20. rokoch 17. storočia boli európske včely medonosné (A. m. mellifera) úspešne zavlečené do Severnej Ameriky na opeľovanie a produkciu medu. Neskôr, v roku 1822, boli zavlečené do Austrálie (14). Pokusy zopakovať pôvodné úspechy zo Severnej Ameriky a Austrálie zlyhali v roku 1839 v Brazílii a v iných tropických oblastiach (15, 16). Verilo sa, že toto zlyhanie pramení z veľmi rozdielneho podnebia na oboch kontinentoch. V roku 1955 sa uskutočnili nové pokusy zahŕňajúce africkú včelu medonosnú (A. m. scutellata), ktorá bola krížená s medonosnými včelami európskeho pôvodu s cieľom vytvoriť hybridný druh, ktorý by lepšie prosperoval v tropickom prostredí a produkoval veľké množstvo vysoko kvalitného medu ( 15 – 18). V nasledujúcom roku však 26 matiek a ich roje afrikanizovaných (hybridných) včiel uniklo z laboratória a napadli veľké časti Ameriky a rozšírili sa o 300 – 500 km ročne (obrázok 1) (15 – 17). Včely dosiahli Mexiko v roku 1986, USA v roku 1990 (Texas) a odvtedy sa rozšírili do mnohých štátov vrátane Kalifornie, Arizony, Utahu, Nového Mexika, Oklahomy, Louisiany, Arkansasu, Alabamy a Floridy (16, 19–22). . Hoci klimatické obmedzenia, najmä chladné zimy, výrazne spomalili šírenie týchto hybridných včiel a v súčasnosti obmedzujú rozsah ich biotopu, stále sa verí, že sú schopné kolonizovať Severnú Ameriku, kde bude ich jedinou prirodzenou bariérou tuhá zima. Tento rozsah sa pravdepodobne bude rozširovať s globálnym nárastom teplôt (16, 23).
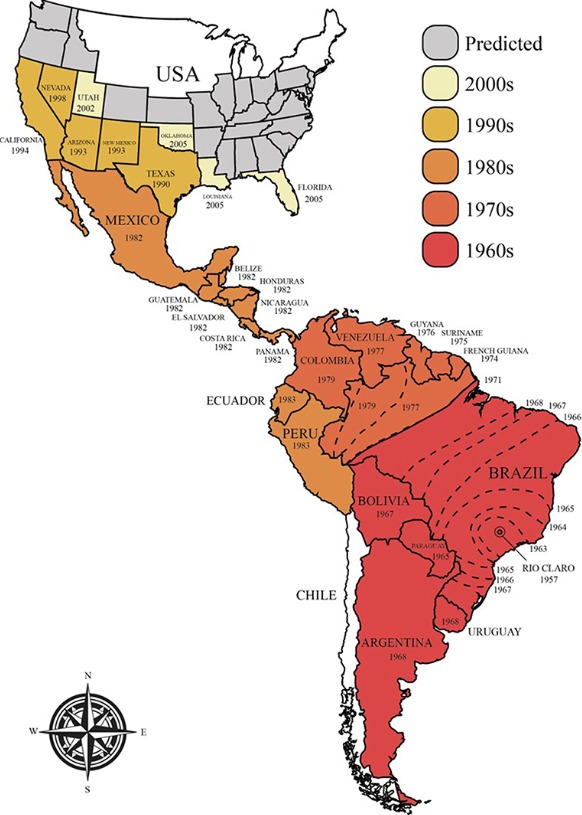
Úspech afrikanizovaných včiel v Amerike sa pripisuje kombinácii ekologických a genetických faktorov, ktoré im poskytli zvýšenú kondíciu v porovnaní s domácimi opeľovačmi (15, 16). Príklady zahŕňajú vyššiu reprodukčnú rýchlosť, kratší vývojový cyklus (t. j. robotniciam trvá 19 – 20 dní namiesto 21 a matkám trvá 14 dní namiesto 16, kým dospejú), vyššia produkcia/početnosť trúdov, vyššia miera úteku (t. j. nútené premiestňovanie kolónií v prípade nedostatku potravy) a vyššia miera rojenia (prirodzená expanzia a rozmnožovanie kolónií; 6–12-krát ročne v prípade dostatku potravy), nižšie potreby skladovania medu, odolnosť voči chorobám a znížená selektivita pri výbere hniezdisk (15, 24–26). Okrem toho sú afrikanizované včely výrazne defenzívnejšie ako iné včely. Prejavuje sa to v ich sklone útočiť s malou stimuláciou, zvýšeným počtom včiel, ktoré spoluútočia vo väčšej vzdialenosti od úľa ako zvyčajne, ich výrazným naliehaním na prenasledovanie votrelcov po dlhšiu dobu a vypúšťaním údajne väčších objemov. z jedu (15, 16). Tieto vlastnosti viedli k tomu, že sú bežne známe ako „včely zabijaky“.
Predpokladá sa, že zvýšená agresivita týchto včelích hybridov spôsobuje značné pokračujúce straty hospodárskych zvierat a problémy so zdravím ľudí, napriek tomu existuje nedostatok spoľahlivých informácií o frekvencii masívnych bodavých udalostí a závažných otravách (8, 27, 28). Tento nedostatok údajov je pravdepodobný preto, že väčšina včelích bodnutí má menší medicínsky význam a uštipnutí jedinci nevyhľadávajú lekársku starostlivosť (8, 27). Okrem toho niekoľko vládnych agentúr zhromažďuje údaje o frekvenciách bodnutia (8) a často zoskupuje všetky uhryznutia a bodnutia zvierat v lekárskych záznamoch z pohotovostných oddelení (29). Napríklad v USA sa vo výročnej správe Americkej asociácie centier na kontrolu jedov uvádza, že v roku 2017 došlo k 41 850 uhryznutiam/uštipnutím zvieratami a štyrom úmrtiam, avšak nedostatok špecifickosti údajov znemožňuje pripísať určitý počet prípadov. na otravy včiel (29). Hoci nedávna správa Centra pre kontrolu a prevenciu chorôb (CDC) ukazuje, že za posledných 5 rokov sa zvýšil počet nehôd a úmrtí bodavým hmyzom (ročný priemer 62 úmrtí), správa kombinuje nehody sršňov, ôs a včiel. spolu (30). Aj keď existuje jedna príkladná správa o otravách suchozemskými zvieratami v Brazílii, kde sa údaje zbierali v priebehu 12 rokov (8, 27). Štúdia zistila, že v rokoch 2001 až 2012 bolo zaznamenaných celkovo 1 192 667 otrav, z ktorých 66 283 (5,6 %) možno pripísať včelám. Pozoruhodné je, že uštipnutie včelou má druhú najvyššiu mieru úmrtnosti (0,33 %; 216 úmrtí), pričom ju prevyšuje iba uštipnutie hadom (0,43 %; 3 394 úmrtí) (27). Štúdia ukázala, že miera úmrtnosti v rokoch 2001 až 2012 neprejavila žiadne významné výkyvy (27). Vzhľadom na významný výskyt včelích bodnutí v Brazílii je pravdepodobné, že podobné problémy verejného zdravia existujú aj v iných krajinách v Amerike s veľkým počtom afrikanizovaných kolónií včiel (27, 28). V skutočnosti sa od ich príchodu do USA objavilo niekoľko správ o úmrtiach po útokoch roja afrikanizovaných včiel (31). Celkovo vzaté, značný počet včelích bodnutí a relatívne vysoká miera úmrtnosti týchto bodnutí naznačujú, že existuje rastúca medicínska potreba inovatívnych možností liečby, ako sú špecifické včelie protijedy na riešenie závažných jedov. Finančné vyhliadky vývoja produktov proti jedu pre trh sú však v súčasnosti neznáme a ťažko predvídateľné.
Včelie bodnutie a jed
Žihadlo má tri funkčne odlišné časti; motorická časť, žíhacia časť a časť súvisiaca s jedom (obrázok 2A) (32–34). V žíhacej časti zohrávajú dôležitú úlohu mandrén a lancety. Prekrývajú ich štvorstenné ostne, ktoré sú rozmiestnené špirálovito pravotočivo. Tento špecifický typ distribúcie hrá zásadnú úlohu pri špirálovej rotácii žihadla v smere hodinových ručičiek počas prenikania žihadla do rany a znižuje penetračnú silu (35). Tieto ostne včele takmer znemožňujú stiahnuť žihadlo z elastického mäsa cicavcov pri úteku (obrázok 2B). Táto situácia môže ľahko viesť k autotómii žihadla, kedy sa žihací aparát a s ním spojené svaly oddelia od zvyšku brucha pri úteku včely od obete (36).
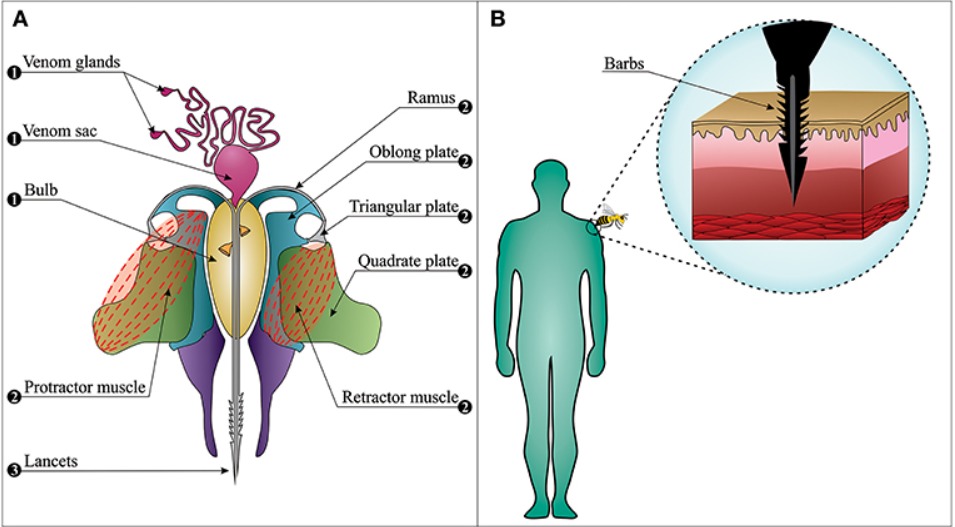
Na rozdiel od všeobecného presvedčenia zostávajú včely robotnice nažive 18–114 hodín po autotomizácii bodnutia a naďalej hrajú svoju úlohu obrancov (37). Keď včela utečie, jej autotomizované žihadlo sa naďalej zasúva do rany po dobu ~30 s (38) a jed môže byť stále dodávaný. Je pozoruhodné, že najmenej 90 % obsahu jedového vrecúška sa doručí v priebehu prvých 20 sekúnd po bodnutí (38) a odstránenie bodnutia (pozri časť Poškodenie včely: Klinické prejavy) 1 minútu po tejto udalosti je nepravdepodobné. znížiť toxicitu vyvolanú jedom. Pri bodnutí sa v priemere dostane 140 – 150 μg jedu a stredná letálna dávka (LD50) včelieho jedu sa pohybuje medzi 2,8 a 3,5 mg jedu na kg telesnej hmotnosti človeka (38 – 41). Dá sa teda špekulovať, že nealergický človek s hmotnosťou 60 – 70 kg má 50 % pravdepodobnosť úmrtia po uštipnutí 1 000 – 1 500 včelami, hoci boli hlásené aj úmrtia spôsobené iba 200 – 500 bodnutiami (38, 42). . Závažnosť otravy je skutočne určená vekom obete, telesnou hmotnosťou, počtom bodnutí a individuálnymi charakteristikami obete (imunitný stav, komorbidity a predchádzajúca senzibilizácia) (43).
Včelí jed je komplexná zmes zlúčenín, ktoré zahŕňajú proteíny, peptidy, aminokyseliny, fosfolipidy, cukry, biogénne amíny, prchavé zlúčeniny, feromóny a veľké množstvo vody (>80%) (44–46). Zloženie včelieho jedu už bolo objasnené omickými technikami (47–49) a frakcionáciou jedu (50–53). V tomto prehľade budú podrobne opísané iba zložky s dôležitými klinickými a terapeutickými účinkami a s dostatočnou podporou literatúry, zatiaľ čo ostatné zlúčeniny včelieho jedu sú uvedené iba v tabuľke 1. Je dôležité zdôrazniť, že včely sú hmyz z radu Hymenoptera, ktorý zahŕňa osy (80). Preto včelie jedy obsahujú niektoré z rovnakých zlúčenín ako jedy osy, ako je adrenalín, dopamín, histamín, hyaluronidáza, noradrenalín, fosfolipázy A2 (PLA2s), fosfolipázy B (PLB) a serotonín (81), zatiaľ čo apamín obsahujú iba včelie jedy. (82), melitín (50) a peptid degranulujúci žírne bunky (MCD) (83, 84).

Melittín je hlavná a najtoxickejšia zlúčenina včelieho jedu, ktorá tvorí 50–60 % celkového jedu (85). Melittín vyvoláva iba menšie alergické reakcie (86), ale spôsobuje väčšinu bolesti spojenej so včelím bodnutím (4), ktorá je vyvolaná priamym a nepriamym pôsobením na primárne nociceptorové bunky. Priame pôsobenie je spôsobené melitínovou aktiváciou termálneho nociceptorového potenciálu vaniloidu 1 (TRPV1) prostredníctvom kaskádovej dráhy PLA2, čo vedie k senzibilizácii primárnych nociceptorov (87–89). Nepriamy účinok je založený na pôsobení melitínu pri tvorbe pórov (obrázok 3), ktorý umožňuje uvoľňovanie látok vyvolávajúcich bolesť, ako sú H+, adenozíntrifosfát (ATP) a 5-hydroxytryptamín (5-HT) zo žírnych buniek. ako aj melitín spôsobuje poškodenie tkaniva, čo vedie k aktivácii receptorov bolesti. Tvorba pórov vyvolaná melitínom môže tiež uvoľňovať mediátory, ako je histamín, bradykinín a ATP, ktoré aktivujú receptory spojené s G-proteínom (GPCR), čo vedie k fosforylácii fosfolipázy C (PLC). PLC štiepi fosfatidylinozitol 4,5-bisfosfátintodiacylglycerol (DAG) a inozitol 1,4,5-trifosfát (IP3). DAG je endogénny aktivátor kanonických kanálov s prechodným receptorovým potenciálom (TRPC), čo vedie k nepriamej excitácii primárnych nociceptívnych neurónov (t.j. bolesti). Podrobnejší prehľad mechanizmu melittínu vyvolávajúceho bolesť možno nájsť inde (4). Melittín je klasifikovaný ako lytický peptid, ktorý je schopný ničiť membránové fosfolipidy, medzi ktoré patria erytrocyty, čo vedie k hemolýze (85, 91). Tento účinok môže byť odvodený od konformačnej modifikácie, kde sa predpokladá, že molekuly melitínu sa viažu kolmo na membrány vytvárajúce póry (90) (obrázok 3). Okrem toho môže melitín zvýšiť aktivitu PLA2 (92). Napríklad aktivita PLA2 bola testovaná s melittínom a bez neho na lecitínových lipozómoch a bolo pozorované, že aktivita PLA2 bola 5-krát vyššia v prítomnosti melitínu (92). Vo včelom jede možno nájsť rôzne izoformy melitínu, ako je melitín-S a melittín-F. Tieto však existujú len v malom množstve (68, 71). Preukázalo sa, že melittín má antimikrobiálnu aktivitu in vitro a in vivo (91), protizápalové účinky in vitro (93), antivírusovú aktivitu in vitro (94) a protirakovinové účinky in vitro a in vivo (95). Nakoniec stojí za zmienku, že melitín možno chemicky syntetizovať, aby sa získali vysoké množstvá peptidu (69, 96, 97).
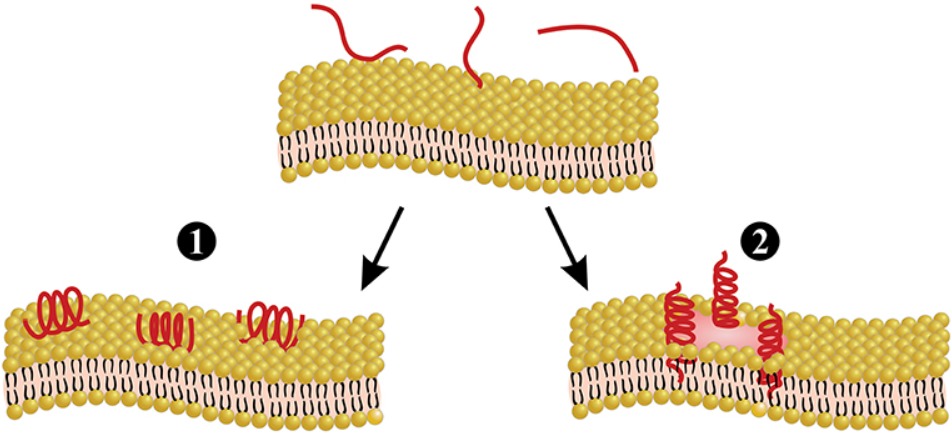
Fosfolipáza A2 (PLA2) je druhou najrozšírenejšou zlúčeninou (10–12 %) a najalergénnejším a najimunogénnejším proteínom vo včelom jede (83). Samotná PLA2 je netoxický proteín (44, 83), ale keď PLA2 vytvorí komplex s melitínom, nazývaný včelí hemolytický faktor, štiepi fosfolipidy bunkovej membrány (98). In vitro má včelí PLA2 niekoľko aktivít, ako sú trypanocídne a antibakteriálne účinky (99, 100), ochrana neurónov spôsobená priónovými proteínmi (101) a protinádorové vlastnosti (102). Okrem toho bola včelia PLA2 schopná znížiť hepatotoxicitu spôsobenú acetaminofénom u myší (103). Fosfolipáza B (PLB) bola tiež hlásená ako prítomná vo včelom jede (75). PLB vykazuje aktivitu PLA1 aj PLA2, pričom je zodpovedná za štiepenie fosfolipidov v polohe sn-1 a sn-2 acylových reťazcov (104), čo zvyšuje aktivitu PLA2 (46). PLB sú tiež dôležitými zložkami hadích jedov (46, 75, 105, 106).
Apamín je ďalší dôležitý peptid vo včelom jede, ktorý tvorí 1–3 % surového jedu a je schopný alostericky a selektívne inhibovať Ca2+-dependentné K+ kanály (SK kanály), nachádzajúce sa v centrálnom nervovom systéme (CNS) (81, 107, 108). Je známe, že iba kanály SK2 a SK3 sú citlivé na apamín, a keď sú zablokované, dochádza k zníženiu oneskorenej hyperpolarizácie buniek, čo vedie k zvýšenému nepretržitému spúšťaniu neurónov v mezencefale a mozočku, čím sa zvyšuje citlivosť buniek na excitačné vstupy (107 , 109). Okrem toho je apamín schopný aktivovať inhibičné muskarínové receptory motorických nervových zakončení (t. j. zníženie neuromuskulárneho prenosu), čo bolo experimentálne skúmané ako potenciálna liečba proti chorobám s vysokou svalovou excitabilitou (110), ako je Parkinsonova choroba (111), učenie deficitná porucha (112) a iné postihnutia (81, 113).
Hyaluronidáza je enzým nachádzajúci sa vo včelom jede (1–3 %), ako aj v mnohých iných živočíšnych jedoch (114–117). Hyaluronidáza je zodpovedná za rýchlu distribúciu toxínov, ktorá je známa aj ako „faktor šírenia“, keďže tento enzým štiepi kyselinu hyalurónovú z extracelulárnej matrice (ECM) (83, 118, 119), čo vedie k rýchlejšiemu a systémovému otráveniu rozrušením tkanív ( 120). Okrem toho sa hyaluronidáza považuje za silný alergén vo včelom jede (121).
Peptid degranulujúci žírne bunky (MCD) sa tiež považuje za dôležitú zložku včelieho jedu na základe jeho schopnosti vyvolať uvoľňovanie histamínu zo žírnych buniek, ktoré majú ústrednú úlohu pri zápaloch a alergiách (122). Vo veľkých množstvách však MCD vykazuje opačný účinok, keď inhibuje degranuláciu žírnych buniek (t. j. inhibíciou uvoľňovania histamínu). MCD teda môže pôsobiť aj ako antialergická molekula (123). Štúdie skutočne preukázali, že MCD peptid vykazuje protizápalovú aktivitu in vitro a in vivo (124, 125).
Okrem vyššie uvedených zložiek včelí jed obsahuje aj amíny, ako sú histamín a katecholamíny (81). Histamín je schopný zvýšiť priepustnosť kapilár, čím prispieva k zápalovej reakcii, zatiaľ čo katecholamíny (t. j. noradrenalín a dopamín) zvyšujú distribúciu včelieho jedu, pretože okrem iných funkcií zvyšujú srdcový výdaj (122).
Čo sa týka iných jedov (105, 126, 127), včelí jed je okrem iných faktorov veľmi náchylný na variabilitu v závislosti od veku včiel, druhu, sociálnych podmienok, geografickej lokalizácie (44). Napríklad mladé robotnice (pásači/strážcovia/ošetrovatelia) majú vyššie hladiny apamínu a nižšie hladiny melitínu v porovnaní so starými robotnicami (pásači/strážcovia). Naproti tomu včelie kráľovné majú nižšie hladiny melitínu a apamínu (128) a vyššie hladiny histamínu (129). Okrem toho mladé včely majú nízke hladiny histamínu, zatiaľ čo vo veku 35 dní majú vysoké hladiny tejto molekuly. Melittín dosahuje maximálnu koncentráciu, keď má včela 4 týždne, a potom počas starnutia včiel klesá; zatiaľ čo promelitín je najrozšírenejší, keď sú včely staré 8–10 dní (130). Hladiny hyaluronidázy sa líšia aj u včelích jedov. Hoci hyaluronidáza môže byť detekovaná ihneď po tom, ako sa kukly vynoria z vajíčok ako dospelých včiel (t. j. eklózia), hladiny enzýmov sa starnutím včiel zvyšujú (131). Zatiaľ čo nízke koncentrácie PLA2 sa nachádzajú počas vyhynutia včiel, postupne sa zvyšujú a najvyššie hladiny dosahujú, keď sú včely staré 7–10 dní (51).
Čo sa týka variácií jedu medzi rôznymi druhmi včiel, africké včely uvoľňujú pri bodnutí malé množstvo jedu s nižším množstvom melitínu a hyaluronidázy a zvýšeným množstvom PLA2, čo možno vysvetliť skutočnosťou, že tieto včely majú menšie jedové žľazy ako európske včely. včely (132–135). Okrem toho môžu mať sezónne zmeny vplyv na obsah včelieho jedu, pretože ročné obdobia ovplyvňujú kvety a plody, a teda aj kŕmenie včiel (104). Produkcia melitínu sa počas leta mení (136), zatiaľ čo produkcia melitínu-S sa zvyšuje počas zimy, čo umožňuje melitínu-S dosiahnuť množstvo 10 % celého jedu (68).
Spôsoby dojenia jedu môžu tiež ovplyvniť zloženie včelieho jedu. Včelí jed možno odobrať extrakciou jedu žliaz alebo elektrickou stimuláciou a jedy zozbierané týmito metódami predstavujú rozdiely v chromatografických profiloch. Prchavé zložky, ako je histamín, môžu zmiznúť, keď sa včelí jed odoberie elektrickou stimuláciou (44, 137). Navyše, prostredníctvom proteomickej analýzy môže byť včelí jed získaný extrakciou žľazy kontaminovaný proteínmi z tkaniva žľazy, takže iba 40 % získaného materiálu tvoria skutočné proteíny včelieho jedu. Vo všeobecnosti však pri použití elektrickej stimulácie viac ako 80 % získaného materiálu tvoria proteíny jedu (48).
Včelie bodnutia: Klinické prejavy
Bodnutia včiel môžu viesť k miernym až závažným klinickým prejavom v závislosti najmä od počtu žihadiel, ktoré obeť dostala. Vek pacienta, hmotnosť, komorbidity a lekárska starostlivosť môžu tiež ovplyvniť závažnosť otravy (28). Navyše, atopickí jedinci (napr. jedinci s astmou alebo alergickou rinitídou) a rodinná anamnéza alergie na včelie bodnutie sú spojené s vyšším výskytom závažných reakcií (138). Typicky možno klinické prejavy otravy včiel rozdeliť na lokálne zápalové reakcie (1), alergické prejavy (2), anafylaktický šok (3) a systémové toxické reakcie (4) (43, 139). (1) Lokálne zápalové reakcie sú charakterizované bolesťou, opuchom (edém a erytém), svrbením a svrbením v mieste bodnutia. Tieto reakcie pociťuje väčšina nealergických jedincov a zvyčajne ustúpia do 24 hodín (39). (2) Alergické reakcie na včelie bodnutie sú závislé od IgE a sú klasifikované ako reakcie z precitlivenosti I. typu. Tieto reakcie sa vyskytujú asi 10 minút po uštipnutí a symptómy sa môžu líšiť v závažnosti. PLA2 sa považuje za hlavnú zlúčeninu, ktorá vyvoláva IgE-senzibilizáciu žírnych buniek, hoci hyaluronidázy a melittín sa tiež považujú za alergény (140) (pozri časť Včelie bodnutie a jed). U alergických pacientov sa môže vyvinúť systémová žihľavka, pruritus, angioedém, vracanie a hnačka (28). (3) V niektorých prípadoch sa alergické reakcie môžu rozvinúť do anafylaktickej reakcie, ktorá vedie k bronchokonstrikcii a anafylaktickému šoku (39). 25 % až 70 % pacientov s alergiami na hmyz vykazuje systémové reakcie, keď sú vystavení alergénu (t. j. včeliemu jedu) (140). Je zaujímavé, že u niektorých nealergických jedincov sa môže vyvinúť anafylaxia včiel v dôsledku systémovej mastocytózy (141–143). Systémová mastocytóza je heterogénna porucha charakterizovaná proliferáciou mastocytov a rozsahom granulácie, ktorá je spôsobená mutáciami v géne c-Kit (rastový faktor pre mastocyty) (144, 145). (4) Systémové toxické reakcie sú charakterizované priamymi toxickými účinkami včelieho jedu, nezávislými od imunitných mechanizmov, ktoré sú známe aj ako reakcie závislé od objemu jedu. Systémové toxické reakcie sa vždy považujú za závažné a sú spôsobené viacerými bodnutiami (asi 50 súčasných bodnutí). Pacienti trpiaci systémovými toxickými reakciami môžu mať únavu, závraty, nevoľnosť, vracanie a hnačku, ktoré sa môžu rozvinúť do poškodenia myokardu, hypertenzie, poškodenia pečene, rabdomyolýzy, hemolýzy, kómy a akútneho zlyhania obličiek (43, 146, 147). K úmrtiam pravdepodobne dôjde, keď obeť dostane asi 500 žihadiel, ktoré sa považujú za nevyhnutné na spôsobenie smrti priamou toxicitou (42), hoci menej bodnutí (30 – 50) sa ukázalo ako smrteľné u detí (148).
Pri bodnutí včelou boli hlásené aj ďalšie zriedkavé klinické prejavy, vrátane periférnej neuritídy (149), Fisherovho syndrómu (150), akútnej zápalovej polyradikuloneuropatie (Guillain-Barrého syndróm) (151), neuropatie zrakového nervu (152), septikémie (153), bilaterálnej empyém (154) a dokonca žihľavka u dieťaťa (12-dňového) dojčeného matkou, ktorú uštipla včela (155).
Súčasná liečba
Vo všeobecnosti existujú tri rôzne scenáre bodnutia včelou, ktoré vyžadujú liečbu. (1) Niekoľko žihadiel na nesenzibilizovanú osobu; (2) jedno alebo viac žihadiel precitliveného človeka; a (3) masívna otrava včiel viacerými bodnutiami (obrázok 4).
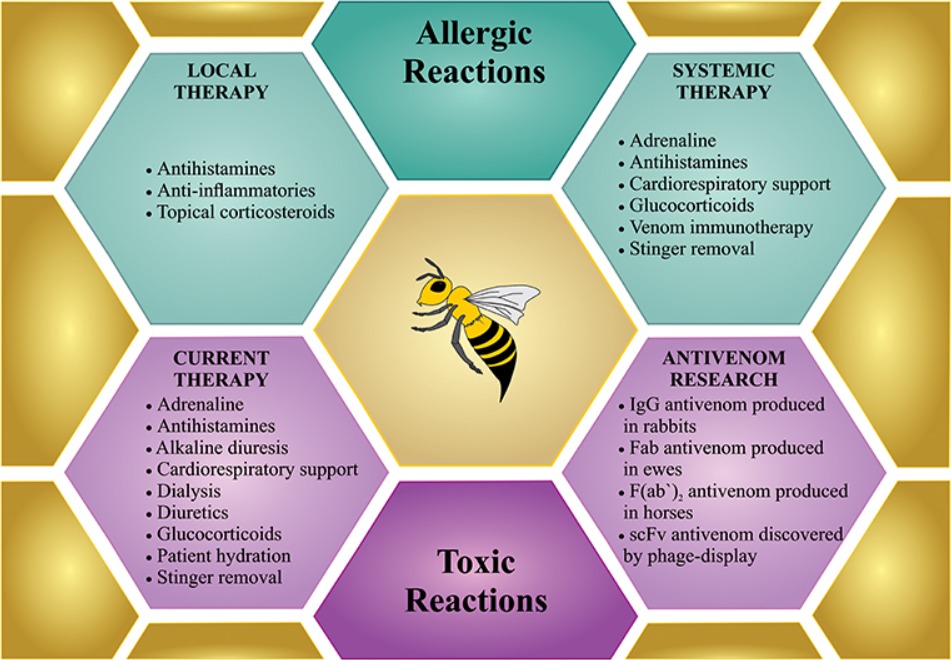
Liečba niekoľkých žihadiel na nesenzibilizovanej osobe
Nesenzibilizovaní ľudia prezentujú iba lokalizovanú reakciu na včelie bodnutie. Pri normálnej reakcii na včelie bodnutie sa koža prejaví ako oblasť bolesti, začervenania a opuchu, ktorá má zvyčajne priemer < 10 cm a normálne zmizne do 24 hodín (156). Experimenty vykonané na morčatách poštípaných včelami, ktorým boli odstránené tkanivá a podrobené histologickej analýze, preukázali iba lokálny výrazný zápal (t. j. edém, vysokú bunkovú infiltráciu a nekrózu) počas 24 hodín po bodnutí (157). Lekárska pomoc je v týchto prípadoch zbytočná, hoci sa odporúča použitie lokálnych kortikosteroidov, ktoré majú protizápalové, imunosupresívne a antimitogénne účinky (158). Pri takzvaných veľkých lokálnych reakciách na bodnutie hmyzom však môže byť oblasť opuchu a začervenania väčšia ako 10 cm v priemere a bolesť môže pretrvávať aj niekoľko dní. Hoci je táto reakcia pravdepodobne alergického pôvodu, nemusí byť nevyhnutne sprostredkovaná IgE. V tejto situácii možno predpísať perorálne antihistaminiká (156).
Liečba precitlivenosti
Ak osobu precitlivenú na včelí jed (t. j. alergika) poštípe aspoň jedna včela, je potrebná okamžitá lekárska pomoc, pretože môže dôjsť k anafylaxii. Väčšina úmrtí, ku ktorým dochádza v tomto prípade, je spôsobená tým, že alergickí jedinci nedostanú lekársku starostlivosť dostatočne rýchlo (159). Preferovaná prvá línia účinku proti anafylaxii sa líši od štúdie k štúdii. Niektoré štúdie uvádzajú ako prvú líniu účinku opatrné zoškrabovanie včelích žihadiel (vyhýbaním sa ťahaniu alebo stláčaniu žihadiel, čo by mohlo viesť k vstreknutiu väčšieho množstva jedu) (160), hoci tento úkon je dôležitý najmä vtedy, ak sa vykoná do 60 s. bodnutie, v ktorom žihadlo vyvrhne všetok svoj jed (39). Iné štúdie uvádzajú, že prvou líniou účinku by malo byť podanie intramuskulárneho adrenalínu (tiež známeho ako epinefrín) a až potom odstránenie žihadla (161). Aj keď sa tieto štúdie nemusia zhodovať v tom, či by odstránenie žihadla malo byť prvou akciou, po ktorej nasleduje adrenalín, alebo naopak, zhodujú sa v tom, že prvým liekom, ktorý sa má použiť, je intramuskulárny adrenalín (39, 160–162). Aj niekoľkominútové oneskorenie v podaní adrenalínu môže viesť k hypoxii alebo smrti. Nedostatočný prístup k vznikajúcemu adrenalínu skutočne zohráva rozhodujúcu úlohu v úmrtnosti a morbidite alergických pacientov. Zvýšilo sa tak povedomie o potrebe adrenalínových autoinjektorov na verejných miestach vrátane škôl, parkov, letísk a nákupných centier (163, 164).
Adrenalín pôsobí ako α a β-agonista. Vďaka svojmu α-1 agonistickému účinku pôsobí ako vazokonstriktor, ktorý zabraňuje a zmierňuje edém dýchacích ciest, hypotenziu a šok. β-1 agonistické účinky adrenalínu sú chronotropné a inotropné a teda zvyšujú rýchlosť a silu srdcových kontrakcií, zatiaľ čo β-2 agonistické účinky adrenalínu vedú k bronchodilatácii (162). Okrem toho β2-adrenergné agonistické účinky adrenalínu tiež zvyšujú intracelulárne hladiny cyklického adenozínmonofosfátu v žírnych bunkách, čo inhibuje ďalšie uvoľňovanie zápalových mediátorov, ako sú histamín, leukotriény a prostaglandín D2 (165). Po podaní adrenalínu medzi ďalšie liečby prvej línie patrí kyslík, intravenózna tekutinová resuscitácia a inhalačné krátkodobo pôsobiace β2 agonisty (161, 166, 167). Liečba druhej línie zvyčajne pozostáva z H1-antihistaminík, H2-antihistaminík a glukokortikoidov, ktoré sa podávajú ako adjuvantná liečba a považujú sa za voliteľné. Antihistaminiká sa odporúčajú len na zmiernenie kožných symptómov, zatiaľ čo glukokortikoidy môžu byť účinné pri liečbe edému dýchacích ciest a môžu zabrániť dlhotrvajúcim symptómom anafylaxie (161, 166).
Preventívnou liečbou pre alergických jedincov je imunoterapia jedom (VIT). VIT pozostáva z očkovania malých zvyšujúcich sa množstiev purifikovaných extraktov jedu u alergického jedinca počas určitého časového obdobia. Výťažky z jedu boli predstavené v 70. rokoch minulého storočia a odvtedy sa VIT stáva čoraz populárnejším. Bolo vyvinutých niekoľko rôznych režimov podávania na skrátenie času potrebného na dosiahnutie udržiavacieho obdobia a na minimalizáciu vedľajších účinkov (168). Podľa Európskej akadémie pre alergiu a klinickú imunológiu (EAACI) sa VIT môže vykonávať s použitím rôznych produktov jedu (purifikovaných a nečistených, vodných alebo depotných) a rôznych liečebných protokolov (konvenčné, klastrové, rýchle a ultrarýchle), podávané subkutánnou alebo sublingválnou cestou (169).
Efektívna VIT obnovuje imunotoleranciu voči alergénom rôznymi mechanizmami: (1) desenzibilizáciou žírnych buniek a bazofilov; (2) potlačenie vrodených lymfoidných buniek (ILC2); (3) aktivácia regulačných T buniek (Tregs), ktoré zvyšujú hladiny interleukínu 10 (IL-10) a transformujúceho rastového faktora-p (TGF-p); (4) a imunoglobulínový bunkový prechod na IgG4 a IgA indukovaný cytokínmi Treg (170). Rozhodnutie, či začať VIT, závisí od presnej diagnózy, posúdenia rizika ďalšej alergickej reakcie u osoby, od miery, do akej alergia ovplyvňuje kvalitu života osoby, od veku osoby a od sprievodných zdravotných stavov, ako aj od toho, či osoba trpí súbežnou poruchou žírnych buniek. Okrem toho by sa mal vziať do úvahy alergénový prípravok (pozri usmernenia EAACI) a podaná dávka, aby sa predišlo nežiaducim účinkom a zabezpečil sa terapeutický úspech (169). V každom prípade je potrebné VIT vykonávať pod lekárskym dohľadom kvôli riziku alergickej reakcie. Štúdia zistila, že takmer jeden z 10 ľudí liečených VIT mal alergickú reakciu na liečbu (171). Nežiaduce účinky sú však zvyčajne mierne a aj keď sa v prípade systémových nežiaducich reakcií odporúča znížiť dávku alergénu, pacienti by nemali prerušiť liečbu, pretože VIT je účinná pri znižovaní rizika následnej systémovej reakcie na uštipnutie včelou. 77–84 % liečených pacientov (169).
Terapia proti masívnemu otráveniu včiel
Počiatočná liečba masívnej otravy včiel má rovnaký priebeh ako v prípade precitlivenosti. Alergické a systémové toxické reakcie je ťažké rozlíšiť, najmä v prvých minútach, a anafylaktický šok je najbezprostrednejším nebezpečenstvom pre pacienta (172). Akonáhle sa však zistí, že k hypersenzitívnej udalosti nedochádza (alebo nielen), začne sa špecifická liečba masívnej otravy včiel. Ideálnou liečbou proti závažným toxickým účinkom včelieho jedu by bol pravdepodobne protijed. Nie sú však k dispozícii žiadne špecifické protijedy, hoci sa vynakladá veľké úsilie (pozri časť Terapia proti jedom novej generácie) (139). Pacienti, ktorí majú viac ako 50 bodnutí, by mali byť monitorovaní, pretože cirkulujúce toxíny jedu môžu v ich tele pretrvávať hodiny alebo dni a môžu mať potenciál spôsobiť oneskorené reakcie. Spočiatku môže byť poštípaná obeť stabilná. O niekoľko hodín neskôr sa však stav obete môže zhoršiť (28, 172, 173). Klinické monitorovanie by sa malo zamerať na hladiny kreatinínu, močovinového dusíka v sére, elektrolytov a myoglobínu, aby sa posúdila funkcia obličiek a riziko rabdomyolýzy (172, 174). Okrem toho na kontrolu rozvoja syndrómu akútnej respiračnej tiesne a acidózy je potrebné monitorovať pH krvi a hladiny kyslíka. Ak pacient vykazuje známky myoglobinúrie, môže sa vykonať intravenózna injekcia hydrogénuhličitanu sodného na alkalizáciu moču (t. j. na urýchlenie vylučovania obličkami). Alkalická diuréza môže zabrániť kryštalizácii myoglobínu v obličkových tubuloch, čo môže nakoniec viesť k akútnemu zlyhaniu obličiek (172). Okrem toho sa často podáva agresívna hydratácia a diuretiká (139, 174). Pacient môže začať s hemo alebo peritoneálnou dialýzou, výmennou transfúziou alebo plazmaferézou, aby sa eliminovali zložky jedu s nízkou molekulovou hmotnosťou, ako je melitín alebo PLA2, alebo ak sa rozvinie akútne zlyhanie obličiek (5, 172).
Protijedová terapia novej generácie
Jednou z prekážok produkcie protilátok imunizačnými postupmi pri terapiách zameraných na otravu včelím jedom je nedostatočná imunogenicita niekoľkých kľúčových toxínov včelieho jedu, ako je melittín. Ako už bolo spomenuté (pozri časť Včelie bodnutie a jed), melitín je lytický faktor bunkovej membrány (85, 175) s malou molekulovou veľkosťou (5, 176, 177), náhodnou konformáciou (178) a veľmi hydrofóbnymi oblasťami (177). , čo vedie k nízkej imunogenicite (6), čo značne komplikuje produkciu účinných včelích protijedov, pretože melitín nedokáže vyvolať silnú protilátkovú odpoveď u imunizovaných zvierat.
Počas posledných desaťročí bolo zaznamenaných niekoľko pokusov vyvinúť účinnú terapiu otravy včiel. V roku 1996 Schumacher a spol. ohlásili prvý pokus o produkciu včelieho jedu na báze heterológnej protilátky. Tu bola produkovaná polyklonálna zmes protilátok imunoglobulínu G (IgG) postupnými imunizáciami králikov purifikovaným PLA2, melitínom alebo surovým včelím jedom a neutralizačné kapacity boli ďalej hodnotené u myší. Pozorovalo sa, že špecifické anti-PLA2 protilátky jasne znížili toxicitu spojenú s PLA2, keď sa toxín myšiam podával samotný. Naopak, po použití surového jedu to nemalo žiadny významný vplyv na letalitu. Aj keď sa použila kombinácia anti-PLA2 a anti-melitínových protilátok, surová letalita jedu sa u myší neznížila, hoci autori identifikovali protilátky viažuce melitín v králičom sére (176).
V roku 1999 Jones a spol. opísali odlišný prístup založený na Fab (fragment antigen binding) protilátkových fragmentoch. V ich štúdii boli waleské ovce postupne imunizované včelím jedom na produkciu IgG, ktoré boli ďalej štiepené papaínom, aby sa získali Fab fragmenty. Pomocou enzýmového imunosorbentného testu (ELISA) výskumníci preukázali, že protijed na báze Fab bol schopný rozpoznať melitín. Okrem toho pomocou štandardných testov účinnosti (ED50) in vivo výskumníci určili, že na neutralizáciu toxických účinkov a na zabránenie úmrtnosti u myší je potrebných 20,5 mg ovčieho antiséra na báze Fab, keď bol protijed predinkubovaný s 1 mg včelí jed (179). Neskôr antijed na báze fragmentu konskej protilátky F(ab‘)2, opísaný Santosom a kol. (180), bolo preukázané, že je účinný pri neutralizácii toxických aktivít včelieho jedu in vitro a in vivo. In vitro bola hemolytická aktivita 1 mg včelieho jedu neutralizovaná ~50 mg protijedu. In vivo bol konský protijed schopný úplne neutralizovať myotoxické účinky včelieho jedu s účinnou dávkou (ED50) 1,11 mg/ml (mg včelieho jedu/ml protijedu) (180). Tiež pomocou imunizácie koní Barraviera a spoluautori nedávno vyvinuli konský protijed na báze F(ab‘)2 s ED50 1,25 mg/ml (181). Táto štúdia tiež vyvinula protokol pre klinické štúdie fázy I/II s použitím vytvoreného konského protijedu (181).
Súčasné spôsoby produkcie protijedov sú založené na postupných imunizáciách rôznych zvierat, po ktorých nasleduje lacná purifikácia IgG odvodených od zvieracej plazmy. Napriek historickému klinickému úspechu dosiahnutému s protijedmi pochádzajúcimi zo zvieracej plazmy, tieto otravové terapie majú tendenciu spôsobovať nepriaznivé účinky v dôsledku ich heterológnej povahy (182, 183). Zistilo sa, že u 6–59 % pacientov po uštipnutí hadom liečených protijedmi získanými z plazmy sa po podaní protijedu vyskytli nežiaduce reakcie so skorým nástupom, zatiaľ čo u 5–23 % pacientov sa vyskytli reakcie s oneskoreným nástupom (sérová choroba), s príznakmi ako horúčka, vyrážka a žihľavka (182, 184). Tieto nežiaduce reakcie súvisiace s jedom sú hlavne výsledkom zloženia a kvality protijedu, formátu protilátky a/alebo celkového množstva proteínu podaného pacientovi (185). Antijedy pochádzajúce z plazmy sú jedinou komerčne dostupnou možnosťou otravovej terapie. Súčasný pokrok dosiahnutý v oblasti biotechnológie a monoklonálnych protilátok však pozitívne prispel k vývoju experimentálnych antivenomov založených na zmesiach špecifických rekombinantných monoklonálnych protilátok (186–188). Hoci tieto experimentálne protijedy ešte len vstúpia do klinického prostredia, predpokladá sa, že envenomingové terapie založené na rekombinantných monoklonálnych protilátkach a fragmentoch protilátok budú jedného dňa uvedené na trh a že ich výroba bude v budúcnosti ekonomicky realizovateľná (189).
V oblasti rekombinantných včelích protijedov Barbosa a kol. boli prví, ktorí informovali o objave úplne ľudských protilátok na báze jednoreťazcových variabilných fragmentov (scFv) získaných prostredníctvom technológie fágového displeja proti melitínu a PLA2. Tieto toxíny pôsobia synergicky a kombinácia monoklonálnych protilátok proti týmto toxínom môže preto nájsť uplatnenie pri liečbe vážneho otravy včiel. Špecifické monoklonálne protilátky proti melitínu a PLA2 sa vybrali z knižnice fágového displeja a ďalej sa vybrali na toxínovú špecificitu pomocou ELISA. Boli objavené dva rôzne scFv klony, pomenované A7 a C12, proti PLA2 a melittínu. Neutralizačné štúdie ukázali, že tieto dva klony boli schopné neutralizovať hemolytickú aktivitu včelieho jedu in vitro v pomere hmotnosti k hmotnosti 3:1 (scFv:včelí jed). Okrem toho rovnaké monoklonálne scFv inhibovali myotoxicitu a oneskorili úmrtnosť u myší vystavených 1,5 LD50 včelieho jedu v rovnakom pomere (190). Neskôr tí istí výskumníci vybrali dve nové monoklonálne protilátky proti melitínu a PLA2 na báze scFv pomocou technológie fágového displeja, pomenované Afribumab 1 a Afribumab 2. Afribumab 1 a 2 preukázali schopnosť inhibovať hemolýzu včelím jedom (0,5 μg) in vitro v pomere hmotnosti k hmotnosti 1:1:1 (včelí jed:Afribumab 1:Afribumab 2). Použitím myší vystavených 2 LD50 včelieho jedu (čo zodpovedá 9,484 μg/g včelieho jedu) sa preukázalo, že kombinácia Afribumabu 1 a 2 s rovnakým pomerom 1:1:1 znižuje edém a predlžuje prežitie myší na viac ako 400 minút (v porovnaní s približne 100 minútami, keď boli myši vystavené iba 2 LD50 včelieho jedu) (191). V kombinácii tieto štúdie ukázali, že technológia fágového displeja môže byť účinnou metodológiou na selekciu protilátok so špecifickosťou proti neimunogénnym zložkám včelieho jedu (napr. melittín). Takéto protilátky nebolo možné ľahko generovať tradičnejšími prístupmi na objavovanie protilátok založených na imunizácii zvierat. Potenciálne by takéto monoklonálne protilátky proti kľúčovým toxínom z včelieho jedu mohli byť formulované do rekombinantného protijedu na liečbu vážneho otravy včiel. Aj keď presné načasovanie účinného podania takéhoto včelieho jedu nemožno predpovedať z dôvodu obmedzených znalostí o toxikokinetike zložiek včelieho jedu u ľudských subjektov, je pravdepodobné, že podanie protijedu by sa malo uskutočniť do 24 hodín, pretože kinetické štúdie na myšiach preukázali, že V tomto období možno včelí jed zistiť v rôznych orgánoch, ako sú obličky (192).
Keďže účinná terapeutická intervencia je nevyhnutná pre najzávažnejšie prípady masívnej otravy včiel a keďže doterajší stav techniky demonštruje použiteľnosť rôznych biotechnologických techník a metodológií objavovania protilátok v tejto oblasti, je pravdepodobné, že vo vývoji rekombinantných protijedov proti včelám dôjde k výraznému pokroku. v najbližších desaťročiach dôjde k otravám. Zdá sa eminentné, že prístupy k návrhu a vývoju proti jedu zo susednej oblasti otravy hadím uhryznutím môžu byť prijaté pri vývoji terapií novej generácie na otravu včelím jedom. Osobitne je opodstatnené skúmanie užitočnosti rôznych formátov monoklonálnych protilátok (vrátane nanoprotilátok) a prípadne väzbových proteínov nezaložených na protilátkach (ako sú DARPíny a iné vznikajúce skeletové proteíny), pretože to môže umožniť návrh rekombinantných produktov proti jedu s prospešnými účinkami. farmakokinetické vlastnosti, ako je rýchla distribúcia a schopnosť prenikať a zacieliť toxíny hlboko do tkanív (182, 193, 194). Takéto výskumy môžu tiež podnietiť skúmanie stratégií výroby s nízkymi nákladmi pre oligoklonálne protilátky (189) alebo stratégií formulácií na zlepšenie stability a predĺženú skladovateľnosť. Oblasťou relevantnou pre ďalší výskum môže byť aj použitie lacných inhibítorov s malými molekulami. Nakoniec je dokonca možné, že snahy v rámci vývoja vylepšených terapeutík proti včelím jedom môžu podporiť výskum a vývoj v oblasti diagnostiky včelieho jedu, čo môže pomôcť stratifikácii pacientov a klinickému rozhodovaniu.
Záverečné poznámky
Útoky afrikanizovaných včiel sa v Brazílii, odkiaľ pochádzajú, považujú za problém verejného zdravia. Dopady tejto vážnej hrozby si všimli aj ďalšie americké krajiny, keďže tieto hybridy včiel sa v súčasnosti šíria po celej Amerike. V dôsledku toho sa pravdepodobne zvýši počet včelích bodnutí a otravy. Riešenie tohto závažného problému si vyžaduje dobre pripravenú lekársku pohotovosť a špecifickú liečbu proti jedom včiel, ako sú napríklad antijedy. K dnešnému dňu existuje vo vedeckej literatúre len niekoľko správ preukazujúcich pozitívne výsledky s použitím imunizácie zvierat a ošetrujúci lekári zatiaľ nemajú k dispozícii žiadny protijed na liečbu vážneho otravy včiel. Možným vysvetlením nedostatku komerčných včelích protijedov je obtiažnosť získania špecifických protilátok proti kľúčovým zložkám včelieho jedu, pretože tieto majú nízku imunogenicitu. Tradičné metódy založené na postupných imunizáciách zvierat preto nedokážu generovať dostatočne vysoké titre protilátok na terapeutické využitie. Naproti tomu technológia fágového displeja sa ukázala ako sľubná metodológia na generovanie protilátok proti kľúčovým včelím toxínom s nízkou imunogenitou. Táto technológia tak môže v budúcnosti umožniť vývoj účinných rekombinantných včelích protijedov (186–188). Táto technológia je však stále celkom nedávnym prírastkom na poli vývoja protijedov a je potrebné ešte veľa úsilia, kým svetlo sveta uzrie účinný protijed na liečbu ťažkých jedov včiel.
Autorské príspevky
FC, IO, TJ, LA, CS a SA napísali časť recenzie a poskytli kritickú spätnú väzbu. FK a TJ pripravili figúrky. MP a AL navrhli recenziu, napísali časť rukopisu a poskytli revízie. JB dal svoje cenné a profesionálne návrhy. Všetci autori prečítali a schválili konečný rukopis.
Financovanie
Ďakujeme Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq, Národná rada pre vedecký a technologický rozvoj, grant č. 307155/2017-0); Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP, São Paulo Research Foundation, grant č. 2017/04724-4, štipendium FC č. 2017/14035-1 a 2018/14158-9 a štipendium ISO 2017/ ISO 2017 03580-9 a 2018/21233-7); nadácia Villum (č. grantu 00025302).
Vyhlásenie o konflikte záujmov
Autori vyhlasujú, že výskum bol vykonaný bez akýchkoľvek obchodných alebo finančných vzťahov, ktoré by mohli byť chápané ako potenciálny konflikt záujmov.
Poďakovanie
JB (1949–2019) zomrel v záverečných fázach prípravy tohto článku. Táto práca je venovaná jeho pamiatke ako vďačnosť za všetky jeho objavy v rámci včelieho protijedu a za jeho mentorstvo. Ďakujeme Cecilie Mullerup Kiel za korektúru rukopisu.
Referencie
1. Engel MS. A new interpretation of the oldest fossil bee (Hymenoptera: Apidae). Novi. (2000) 2000:1–11. doi: 10.1206/0003-0082(2000)3296<0001:ANIOTO>2.0.CO;2
CrossRef Full Text | Google Scholar
2. Mizrahi A, Lensky Y. Bee Products: Properties, Applications, and Apitherapy. Tel Aviv: Springer Science & Business Media (2013).
3. Hoover SE, Ovinge LP. Pollen collection, honey production, and pollination services: managing honey bees in an agricultural setting. J Econ Entomol. (2018) 111:1509–16. doi: 10.1093/jee/toy125
CrossRef Full Text | Google Scholar
4. Chen J, Guan S-M, Sun W, Fu H. Melittin, the major pain-producing substance of bee venom. Neurosci Bull. (2016) 32:265–72. doi: 10.1007/s12264-016-0024-y
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Schumacher MJ, Egen NB. Significance of Africanized bees for public health: a review. Arch Intern Med. (1995) 155:2038–43. doi: 10.1001/archinte.155.19.2038
PubMed Abstract | CrossRef Full Text | Google Scholar
6. King TP, Coscia MR, Kochoumian L. Structure-immunogenicity relationship of melittin and its N-terminal truncated analogs. Biochemistry. (1993) 32:3506–10. doi: 10.1021/bi00064a039
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gallai N, Salles J-M, Settele J, Vaissière BE. Economic valuation of the vulnerability of world agriculture confronted with pollinator decline. Ecol Econ. (2009) 68:810–21. doi: 10.1016/j.ecolecon.2008.06.014
CrossRef Full Text | Google Scholar
8. Schmidt JO. Clinical consequences of toxic envenomations by Hymenoptera. Toxicon. (2018) 150:96–104. doi: 10.1016/j.toxicon.2018.05.013
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Crane E. The World History of Beekeeping and Honey Hunting. New York, NY: Routledge (1999).
10. Bloch G, Francoy TM, Wachtel I, Panitz-Cohen N, Fuchs S, Mazar A. Industrial apiculture in the Jordan valley during Biblical times with Anatolian honeybees. Proc Natl Acad Sci USA. (2010) 107:11240–4. doi: 10.1073/pnas.1003265107
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Oxley PR, Oldroyd BP. Chapter 3–the genetic architecture of honeybee breeding. Adv Insect Physiol. 39:83–118. doi: 10.1016/B978-0-12-381387-9.00003-8
CrossRef Full Text | Google Scholar
12. Harpur BA, Minaei S, Kent CF, Zayed A. Management increases genetic diversity of honey bees via admixture. Mol Ecol. (2012) 21:4414–21. doi: 10.1111/j.1365-294X.2012.05614.x
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Whitfield CW, Behura SK, Berlocher SH, Clark AG, Johnston JS, Sheppard WS, et al. Thrice out of Africa: ancient and recent expansions of the honey bee, Apis mellifera. Science. (2006) 314:642–5. doi: 10.1126/science.1132772
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Crosby AW. Ecological Imperialism: The Biological Expansion of Europe, 900–1900. Cambridge: Cambridge University Press (2004).
15. Scott Schneider S, DeGrandi-Hoffman G, Smith DR. The African honey bee: factors contributing to a successful biological invasion. Ann Rev Entomol. (2004) 49:351–76. doi: 10.1146/annurev.ento.49.061802.123359
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Ferreira RS Jr, Almeida RAMB, Barraviera SRCS, Barraviera B. Historical perspective and human consequences of Africanized bee stings in the Americas. J Toxicol Environ Health B. (2012) 15:97–108. doi: 10.1080/10937404.2012.645141
PubMed Abstract | CrossRef Full Text | Google Scholar
17. Kumschick S, Devenish A, Kenis M, Rabitsch W, Richardson DM, Wilson JRU. Intentionally introduced terrestrial invertebrates: patterns, risks, and options for management. Biol Invasions. (2016) 18:1077–88. doi: 10.1007/s10530-016-1086-5
CrossRef Full Text | Google Scholar
18. Kerr WE. The history of the introduction of African bees in Brazil. South African Bee J. (1967) 39:33–5.
19. Rinderer TE, Oldroyd BP, Sheppard WS. Africanized bees in the US. Sci Am. (1993) 269:84–90. doi: 10.1038/scientificamerican1293-84
CrossRef Full Text | Google Scholar
20. Lin W, McBroome J, Rehman M, Johnson BR. Africanized bees extend their distribution in California. PLoS ONE. (2018) 13:e0190604. doi: 10.1371/journal.pone.0190604
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Rangel J, Giresi M, Pinto MA, Baum KA, Rubink WL, Coulson RN, et al. Africanization of a feral honey bee (Apis mellifera) population in South Texas: does a decade make a difference? Ecol Evol. (2016) 6:2158–69. doi: 10.1002/ece3.1974
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Portman ZM, Tepedino VJ, Tripodi AD, Szalanski AL, Durham SL. Local extinction of a rare plant pollinator in Southern Utah (USA) associated with invasion by Africanized honey bees. Biol Invasions. (2018) 20:593–606. doi: 10.1007/s10530-017-1559-1
CrossRef Full Text | Google Scholar
23. Harrison JF, Fewell JH, Anderson KE, Loper GM. Environmental physiology of the invasion of the Americas by Africanized honeybees. Integr Comp Biol. (2006) 46:1110–22. doi: 10.1093/icb/icl046
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Caron DM. Africanized Honey Bees in the Americas. Medina: AI Root Co. (2001).
25. Schmidt JO, Hurley R. Selection of nest cavities by Africanized and European honey bees. Apidologie. (1995) 26:467–75. doi: 10.1051/apido:19950603
CrossRef Full Text | Google Scholar
26. Winston ML. The biology and management of Africanized honey bees. Ann Rev Entomol. (1992) 37:173–93. doi: 10.1146/annurev.en.37.010192.001133
CrossRef Full Text | Google Scholar
27. Chippaux J-P. Epidemiology of envenomations by terrestrial venomous animals in Brazil based on case reporting: from obvious facts to contingencies. J Venom Anim Toxins. (2015) 21:13. doi: 10.1186/s40409-015-0011-1
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Fan HW, Kalil J. Massive bee envenomation. In: Brent J, Burkhart K, Dargan P, Hatten B, Megarbane B, Palmer R, White J, editors. Critical Care Toxicology: Diagnosis and Management of the Critically Poisoned Patient. Cham: Springer (2017). p. 2627–36.
29. Gummin DD, Mowry JB, Spyker DA, Brooks DE, Osterthaler KM, Banner W. 2017 Annual report of the american association of poison control centers‘ national poison data system (NPDS): 35th annual report. Clin Toxicol. (2018) 56:1213–415. doi: 10.1080/15563650.2018.1533727
PubMed Abstract | CrossRef Full Text | Google Scholar
30. CDC. QuickStats: Number of deaths from hornet, wasp, and bee stings, among males and females—National vital statistics system, United States, 2000–2017. MMWR Morb Mortal Wkly Rep. (2019) 68:649. doi: 10.15585/mmwr.mm6829a5
CrossRef Full Text | Google Scholar
31. Hughes RL. A fatal case of acute renal failure from envenoming syndrome after massive bee attack: a case report and literature review. Am J Foren Med Pathol. (2019) 40:52–7. doi: 10.1097/PAF.0000000000000451
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Bücherl W, Buckley EE, Deulofeu V. Venomous Animals and Their Venoms. Academic Press (1968). Available online at: https://www.elsevier.com/books/venomous-animals-and-their-venoms/bucherl/978-1-4832-2949-2 (accessed April 8, 2019).
33. Zhao Z-L, Zhao H-P, Ma G-J, Wu C-W, Yang K, Feng X-Q. Structures, properties, and functions of the stings of honey bees and paper wasps: a comparative study. Biol Open. (2015) 4:921–8. doi: 10.1242/bio.012195
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Bridges AR, Owen MD. The morphology of the honey bee (Apis mellifera L.) venom gland and reservoir. J Morphol. (1984) 181:69–86. doi: 10.1002/jmor.1051810107
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Wu J, Yan S, Zhao J, Ye Y. Barbs Facilitate the Helical Penetration of Honeybee (Apis mellifera Ligustica) Stingers. PLoS ONE. (2014) 9:e103823. doi: 10.1371/journal.pone.0103823
PubMed Abstract | CrossRef Full Text | Google Scholar
36. Hermann HR, Blum MS. Defensive mechanisms in the social hymenoptera. Soc Insects. (1981) 2:77–197. doi: 10.1016/B978-0-12-342202-6.50009-5
CrossRef Full Text | Google Scholar
37. Nouvian M, Reinhard J, Giurfa M. The defensive response of the honeybee Apis mellifera. J Exp Biol. (2016) 219:3505–17. doi: 10.1242/jeb.143016
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Schumacher MJ, Tveten MS, Egen NB. Rate and quantity of delivery of venom from honeybee stings. J Allergy Clin Immunol. (1994) 93:831–5. doi: 10.1016/0091-6749(94)90373-5
PubMed Abstract | CrossRef Full Text | Google Scholar
39. Fitzgerald KT, Flood AA. Hymenoptera Stings. Clin Tech Small Anim Pract. (2006) 21:194–204. doi: 10.1053/j.ctsap.2006.10.002
PubMed Abstract | CrossRef Full Text | Google Scholar
40. Schumacher MJ, Schmidt JO, Egen NB. Lethality of “killer” bee stings. Nature. (1989) 337:413. doi: 10.1038/337413a0
PubMed Abstract | CrossRef Full Text | Google Scholar
41. Ali MAA-SM. Studies on bee venom and its medical uses. Int J Adv Res Technol. (2012) 1:69–83.
42. França FO, Benvenuti LA, Fan HW, Dos Santos DR, Hain SH, Picchi-Martins FR, et al. Severe and fatal mass attacks by “killer” bees (Africanized honey bees–Apis mellifera scutellata) in Brazil: clinicopathological studies with measurement of serum venom concentrations. Q J Med. (1994) 87:269–82.
PubMed Abstract | Google Scholar
43. Toledo LFM de, Moore DCBC, Caixeta DM da L, Salú MDS, Farias CVB, Azevedo ZMA de. Multiple bee stings, multiple organs involved: a case report. Rev Soc Bras Med Trop. (2018) 51:560–2. doi: 10.1590/0037-8682-0341-2017
PubMed Abstract | CrossRef Full Text | Google Scholar
44. Abd El-Wahed AA, Khalifa SAM, Sheikh BY, Farag MA, Saeed A, Larik FA, et al. Chapter 13–bee venom composition: from Chemistry to biological activity. In Atta-ur-Rahman editor. Studies in Natural Products Chemistry. Oxford: Elsevier (2017). p. 459–84.
45. Szókán G, Horváth J, Almás M, Saftics G, Palócz A. Liquid chromatographic analysis and separation of polypeptide components from honey bee venoms. J Liq Chromatogr. (1994) 17:3333–49. doi: 10.1080/10826079408013516
CrossRef Full Text | Google Scholar
46. Hossen MS, Shapla UM, Gan SH, Khalil MI. Impact of bee venom enzymes on diseases and immune responses. Molecules. (2016) 22:1–16. doi: 10.3390/molecules22010025
PubMed Abstract | CrossRef Full Text | Google Scholar
47. Danneels EL, Van Vaerenbergh M, Debyser G, Devreese B, de Graaf DC. Honeybee venom proteome profile of queens and winter bees as determined by a mass spectrometric approach. Toxins. (2015) 7:4468–83. doi: 10.3390/toxins7114468
PubMed Abstract | CrossRef Full Text | Google Scholar
48. Li R, Zhang L, Fang Y, Han B, Lu X, Zhou T, et al. Proteome and phosphoproteome analysis of honeybee (Apis mellifera) venom collected from electrical stimulation and manual extraction of the venom gland. BMC Genom. (2013) 14:766. doi: 10.1186/1471-2164-14-766
PubMed Abstract | CrossRef Full Text | Google Scholar
49. Resende VMF, Vasilj A, Santos KS, Palma MS, Shevchenko A. Proteome and phosphoproteome of Africanized and European honeybee venoms. Proteomics. (2013) 13:2638–48. doi: 10.1002/pmic.201300038
PubMed Abstract | CrossRef Full Text | Google Scholar
50. Teoh ACL, Ryu K-H, Lee EG. One-step purification of melittin derived from Apis mellifera bee venom. J Microbiol Biotechnol. (2017) 27:84–91. doi: 10.4014/jmb.1608.08042
PubMed Abstract | CrossRef Full Text | Google Scholar
51. Owen MD, Pfaff LA, Reisman RE, Wypych J. Phospholipase A2 in venom extracts from honey bees (Apis mellifera L.) of different ages. Toxicon. (1990) 28:813–20. doi: 10.1016/S0041-0101(09)80004-4
PubMed Abstract | CrossRef Full Text | Google Scholar
52. Dotimas EM, Hamid KR, Hider RC, Ragnarsson U. Isolation and structure analysis of bee venom mast cell degranulating peptide. Biochim Biophys Acta. (1987) 911:285–93. doi: 10.1016/0167-4838(87)90069-0
PubMed Abstract | CrossRef Full Text | Google Scholar
53. Banks BE, Dempsey CE, Pearce FL, Vernon CA, Wholley TE. New methods of isolating been venom peptides. Anal Biochem. (1981) 116:48–52. doi: 10.1016/0003-2697(81)90320-1
PubMed Abstract | CrossRef Full Text | Google Scholar
54. Ohashi K, Sawata M, Takeuchi H, Natori S, Kubo T. Molecular cloning of cDNA and analysis of expression of the gene for alpha-glucosidase from the hypopharyngeal gland of the honeybee Apis mellifera L. Biochem Biophys Res Commun. (1996) 221:380–5. doi: 10.1006/bbrc.1996.0604
PubMed Abstract | CrossRef Full Text | Google Scholar
55. Kubo T, Sasaki M, Nakamura J, Sasagawa H, Ohashi K, Takeuchi H, et al. Change in the expression of hypopharyngeal-gland proteins of the worker honeybees (Apis mellifera L.) with age and/or role. J Biochem. (1996) 119:291–5. doi: 10.1093/oxfordjournals.jbchem.a021237
CrossRef Full Text | Google Scholar
56. Hoffman DR, Weimer ET, Sakell RH, Schmidt M. Sequence and characterization of honeybee venom acid phosphatase. J Allergy Clin Immunol. (2005) 115:S107. doi: 10.1016/j.jaci.2004.12.442
CrossRef Full Text | Google Scholar
57. Shkenderov S, Koburova K. Adolapin–a newly isolated analgetic and anti-inflammatory polypeptide from bee venom. Toxicon. (1982) 20:317–21. doi: 10.1016/0041-0101(82)90234-3
PubMed Abstract | CrossRef Full Text | Google Scholar
58. Haux P, Sawerthal H, Habermann E. Sequence analysis of bee venom neurotoxin (apamine) from its tryptic and chymotryptic cleavage products. Hoppe-Seyler’s Z Physiol Chem. (1967) 348:737–8.
PubMed Abstract | Google Scholar
59. Kettner A, Hughes GJ, Frutiger S, Astori M, Roggero M, Spertini F, et al. Api m 6: a new bee venom allergen. J Allergy Clin Immunol. (2001) 107:914–20. doi: 10.1067/mai.2001.113867
PubMed Abstract | CrossRef Full Text | Google Scholar
60. Vick JA, Shipman WH, Brooks R. Beta adrenergic and anti-arrhythmic effects of cardiopep, a newly isolated substance from whole bee venom. Toxicon. (1974) 12:139–44. doi: 10.1016/0041-0101(74)90237-2
PubMed Abstract | CrossRef Full Text | Google Scholar
61. Blank S, Seismann H, Bockisch B, Braren I, Cifuentes L, McIntyre M, et al. Identification, recombinant expression, and characterization of the 100 kDa high molecular weight Hymenoptera venom allergens Api m 5 and Ves v 3. J Immunol. (2010) 184:5403–13. doi: 10.4049/jimmunol.0803709
PubMed Abstract | CrossRef Full Text | Google Scholar
62. Gmachl M, Kreil G. Bee venom hyaluronidase is homologous to a membrane protein of mammalian sperm. Proc Natl Acad Sci USA. (1993) 90:3569. doi: 10.1073/pnas.90.8.3569
PubMed Abstract | CrossRef Full Text | Google Scholar
63. Peiren N, de Graaf DC, Brunain M, Bridts CH, Ebo DG, Stevens WJ, et al. Molecular cloning and expression of icarapin, a novel IgE-binding bee venom protein. FEBS Lett. (2006) 580:4895–9. doi: 10.1016/j.febslet.2006.08.005
PubMed Abstract | CrossRef Full Text | Google Scholar
64. Peiren N, Vanrobaeys F, de Graaf DC, Devreese B, Van Beeumen J, Jacobs FJ. The protein composition of honeybee venom reconsidered by a proteomic approach. Biochim Biophys Acta. (2005) 1752:1–5. doi: 10.1016/j.bbapap.2005.07.017
PubMed Abstract | CrossRef Full Text | Google Scholar
65. Schmitzová J, Klaudiny J, Albert S, Schröder W, Schreckengost W, Hanes J, et al. A family of major royal jelly proteins of the honeybee Apis mellifera L. Cell Mol Life Sci. (1998) 54:1020–30. doi: 10.1007/s000180050229
PubMed Abstract | CrossRef Full Text | Google Scholar
66. Klaudiny J. MRJP9, an ancient protein of the honeybee MRJP family with non-nutritional function. J Apicult Res. (2007) 46:99–104. doi: 10.3896/IBRA.1.46.2.06
CrossRef Full Text | Google Scholar
67. Haux P. Amino acid sequence of MCD-peptide, a specific mast cell-degranulating peptide from bee venom. Hoppe-Seyler’s Z Physiol Chem. (1969) 350:536–46. doi: 10.1515/bchm2.1969.350.1.536
PubMed Abstract | CrossRef Full Text | Google Scholar
68. Sciani JM, Marques-Porto R, Lourenço Junior A, Orsi R de O, Ferreira Junior RS, Barraviera B, et al. Identification of a novel melittin isoform from Africanized Apis mellifera venom. Peptides. (2010) 31:1473–9. doi: 10.1016/j.peptides.2010.05.001
PubMed Abstract | CrossRef Full Text | Google Scholar
69. Tosteson MT, Levy JJ, Caporale LH, Rosenblatt M, Tosteson DC. Solid-phase synthesis of melittin: purification and functional characterization. Biochemistry. (1987) 26:6627–31. doi: 10.1021/bi00395a010
PubMed Abstract | CrossRef Full Text | Google Scholar
70. Schröder E, Lübke K, Lehmann M, Beetz I. Haemolytic activity and action on the surface tension of aqueous solutions of synthetic melittins and their derivatives. Experientia. (1971) 27:764–5. doi: 10.1007/BF02136851
PubMed Abstract | CrossRef Full Text | Google Scholar
71. Gauldie J, Hanson JM, Shipolini RA, Vernon CA. The structures of some peptides from bee venom. Eur J Biochem. (1978) 83:405–10. doi: 10.1111/j.1432-1033.1978.tb12106.x
PubMed Abstract | CrossRef Full Text | Google Scholar
72. Lowy PH, Sarmiento L, Mitchell HK. Polypeptides minimine and melittin from bee venom: effects on Drosophila. Arch Biochem Biophys. (1971) 145:338–43. doi: 10.1016/0003-9861(71)90044-0
PubMed Abstract | CrossRef Full Text | Google Scholar
73. Shipolini RA, Callewaert GL, Cottrell RC, Vernon CA. The amino-acid sequence and carbohydrate content of phospholipase A2 from bee venom. Eur J Biochem. (1974) 48:465–76. doi: 10.1111/j.1432-1033.1974.tb03787.x
PubMed Abstract | CrossRef Full Text | Google Scholar
74. Kuchler K, Gmachl M, Sippl MJ, Kreil G. Analysis of the cDNA for phospholipase A2 from honeybee venom glands. The deduced amino acid sequence reveals homology to the corresponding vertebrate enzymes. Eur J Biochem. (1989) 184:249–54. doi: 10.1111/j.1432-1033.1989.tb15014.x
PubMed Abstract | CrossRef Full Text | Google Scholar
75. Doery HM, Pearson JE. Phospholipase B in snake venoms and bee venom. Biochem J. (1964) 92:599–602. doi: 10.1042/bj0920599
PubMed Abstract | CrossRef Full Text | Google Scholar
76. Meng Y, Yang XX, Sheng YX, Zhang JL, Yu DQ. A novel peptide from Apis mellifera and solid-phase synthesis of its analogue. Chin Chem Lett. (2012) 23:1161–4. doi: 10.1016/j.cclet.2012.09.003
CrossRef Full Text | Google Scholar
77. Mourelle D, Brigatte P, Bringanti LDB, De Souza BM, Arcuri HA, Gomes PC, et al. Hyperalgesic and edematogenic effects of Secapin-2, a peptide isolated from Africanized honeybee (Apis mellifera) venom. Peptides. (2014) 59:42–52. doi: 10.1016/j.peptides.2014.07.004
PubMed Abstract | CrossRef Full Text | Google Scholar
78. Georgieva D, Greunke K, Betzel C. Three-dimensional model of the honeybee venom allergen Api m 7: structural and functional insights. Mol BioSyst. (2010) 6:1056. doi: 10.1039/b923127g
PubMed Abstract | CrossRef Full Text | Google Scholar
79. Ovchinnikov YA, Miroshnikov AI, Kudelin AB, Kostina MB, Boikov VA, Magazanik LG, et al. Structure and presynaptic activity of tertiapin, a neurotoxin from honeybee venom. Bioorganicheskaya Khimiya. (1980) 6:359–65.
80. Vetter RS, Visscher PK. Bites and stings of medically important venomous arthropods. Int J Dermatol. (1998) 37:481–96. doi: 10.1046/j.1365-4362.1998.00455.x
PubMed Abstract | CrossRef Full Text | Google Scholar
81. Moreno M, Giralt E. Three valuable peptides from bee and wasp venoms for therapeutic and biotechnological use: melittin, apamin and mastoparan. Toxins. (2015) 7:1126–50. doi: 10.3390/toxins7041126
PubMed Abstract | CrossRef Full Text | Google Scholar
82. Ramalingam K, Snyder GH. Selective disulfide formation in truncated apamin and sarafotoxin. Biochemistry. (1993) 32:11155–61. doi: 10.1021/bi00092a027
PubMed Abstract | CrossRef Full Text | Google Scholar
83. Elieh Ali Komi D, Shafaghat F, Zwiener RD. Immunology of bee venom. Clin Rev Allergy Immunol. (2018) 54:386–96. doi: 10.1007/s12016-017-8597-4
PubMed Abstract | CrossRef Full Text | Google Scholar
84. Buku A. Mast cell degranulating (MCD) peptide: a prototypic peptide in allergy and inflammation. Peptides. (1999) 20:415–20. doi: 10.1016/S0196-9781(98)00167-3
PubMed Abstract | CrossRef Full Text | Google Scholar
85. Raghuraman H, Chattopadhyay A. Melittin: a membrane-active peptide with diverse functions. Biosci Rep. (2007) 27:189–223. doi: 10.1007/s10540-006-9030-z
PubMed Abstract | CrossRef Full Text | Google Scholar
86. Paull BR, Yunginger JW, Gleich GJ. Melittin: an allergen of honeybee venom. J Allergy Clin Immunol. (1977) 59:334–8. doi: 10.1016/0091-6749(77)90056-2
PubMed Abstract | CrossRef Full Text | Google Scholar
87. Ding J, Xiao Y, Lu D, Du Y-R, Cui X-Y, Chen J. Effects of SKF-96365, a TRPC inhibitor, on melittin-induced inward current and intracellular Ca2+ rise in primary sensory cells. Neurosci Bull. (2011) 27:135–42. doi: 10.1007/s12264-011-1018-4
PubMed Abstract | CrossRef Full Text | Google Scholar
88. Hao J, Liu M-G, Yu Y-Q, Cao F-L, Li Z, Lu Z-M, et al. Roles of peripheral mitogen-activated protein kinases in melittin-induced nociception and hyperalgesia. Neuroscience. (2008) 152:1067–75. doi: 10.1016/j.neuroscience.2007.12.038
PubMed Abstract | CrossRef Full Text | Google Scholar
89. Ding J, Zhang J-R, Wang Y, Li C-L, Lu D, Guan S-M, et al. Effects of a non-selective TRPC channel blocker, SKF-96365, on melittininduced spontaneous persistent nociception and inflammatory pain hypersensitivity. Neurosci Bull. (2012) 28:173–81. doi: 10.1007/s12264-012-1213-y
PubMed Abstract | CrossRef Full Text | Google Scholar
90. van den Bogaart G, Guzmán JV, Mika JT, Poolman B. On the mechanism of pore formation by melittin. J Biol Chem. (2008) 283:33854–7. doi: 10.1074/jbc.M805171200
PubMed Abstract | CrossRef Full Text | Google Scholar
91. Memariani H, Memariani M, Shahidi-Dadras M, Nasiri S, Akhavan MM, Moravvej H. Melittin: from honeybees to superbugs. Appl Microbiol Biotechnol. (2019) 103:3265–76. doi: 10.1007/s00253-019-09698-y
PubMed Abstract | CrossRef Full Text | Google Scholar
92. Mollay C, Kreil G. Enhancement of bee venom phospholipase A2 activity by melittin, direct lytic factor from cobra venom and polymyxin B. FEBS Lett. (1974) 46:141–4. doi: 10.1016/0014-5793(74)80354-6
PubMed Abstract | CrossRef Full Text | Google Scholar
93. Moon D-O, Park S-Y, Lee K-J, Heo M-S, Kim K-C, Kim M-O, et al. Bee venom and melittin reduce proinflammatory mediators in lipopolysaccharide-stimulated BV2 microglia. Int Immunopharmacol. (2007) 7:1092–101. doi: 10.1016/j.intimp.2007.04.005
PubMed Abstract | CrossRef Full Text | Google Scholar
94. Baghian A, Jaynes J, Enright F, Kousoulas KG. An amphipathic alpha-helical synthetic peptide analogue of melittin inhibits herpes simplex virus-1. (HSV-1)-induced cell fusion and virus spread. Peptides. (1997) 18:177–83. doi: 10.1016/S0196-9781(96)00290-2
PubMed Abstract | CrossRef Full Text | Google Scholar
95. Oršolić N. Bee venom in cancer therapy. Cancer Metastasis Rev. (2012) 31:173–94. doi: 10.1007/s10555-011-9339-3
PubMed Abstract | CrossRef Full Text | Google Scholar
96. Juvvadi P, Vunnam S, Merrifield RB. Synthetic melittin, its enantio, retro, and retroenantio isomers, and selected chimeric analogs: their antibacterial, hemolytic, and lipid bilayer action. J Am Chem Soc. (1996) 118:8989–97. doi: 10.1021/ja9542911
CrossRef Full Text | Google Scholar
97. Sun X, Chen S, Li S, Yan H, Fan Y, Mi H. Deletion of two C-terminal Gln residues of 12-26-residue fragment of melittin improves its antimicrobial activity. Peptides. (2005) 26:369–75. doi: 10.1016/j.peptides.2004.10.004
PubMed Abstract | CrossRef Full Text | Google Scholar
98. Mingarro I, Pérez-Payá E, Pinilla C, Appel JR, Houghten RA, Blondelle SE. Activation of bee venom phospholipase A2 through a peptide-enzyme complex. FEBS Lett. (1995) 372:131–4. doi: 10.1016/0014-5793(95)00964-B
PubMed Abstract | CrossRef Full Text | Google Scholar
99. Boutrin M-CF, Foster HA, Pentreath VW. The effects of bee (Apis mellifera) venom phospholipase A2 on Trypanosoma brucei brucei and enterobacteria. Exp Parasitol. (2008) 119:246–51. doi: 10.1016/j.exppara.2008.02.002
PubMed Abstract | CrossRef Full Text | Google Scholar
100. Leandro LF, Mendes CA, Casemiro LA, Vinholis AHC, Cunha WR, de Almeida R, et al. Antimicrobial activity of apitoxin, melittin and phospholipase A2 of honey bee (Apis mellifera) venom against oral pathogens. An Acad Bras Cienc. (2015) 87:147–55. doi: 10.1590/0001-3765201520130511
CrossRef Full Text | Google Scholar
101. Jeong J-K, Moon M-H, Bae B-C, Lee Y-J, Seol J-W, Park S-Y. Bee venom phospholipase A2 prevents prion peptide induced-cell death in neuronal cells. Int J Mol Med. (2011) 28:867–73. doi: 10.3892/ijmm.2011.730
PubMed Abstract | CrossRef Full Text | Google Scholar
102. Son DJ, Lee JW, Lee YH, Song HS, Lee CK, Hong JT. Therapeutic application of anti-arthritis, pain-releasing, and anti-cancer effects of bee venom and its constituent compounds. Pharmacol Ther. (2007) 115:246–70. doi: 10.1016/j.pharmthera.2007.04.004
PubMed Abstract | CrossRef Full Text | Google Scholar
103. Kim H, Keum DJ, Kwak J won, Chung H-S, Bae H. Bee venom phospholipase A2 protects against acetaminophen-induced acute liver injury by modulating regulatory T cells and IL-10 in mice. PLoS ONE. (2014) 9:e114726. doi: 10.1371/journal.pone.0114726
PubMed Abstract | CrossRef Full Text | Google Scholar
104. Abusabbah M, Lau WH, Mahmoud ME, Salih AM, Omar D. Prospects of using carbohydrates as supplemented-diets and protein rich mixture as alternative-diet to improve the quality of venom produced by Apis cerana L. J Entomol Zool Stud. (2016) 4:23–6.
105. Oliveira IS de, Cardoso IA, Bordon K de CF, Carone SEI, Boldrini-França J, Pucca MB, et al. Global proteomic and functional analysis of Crotalus durissus collilineatus individual venom variation and its impact on envenoming. J Proteomics. (2019) 191:153–65. doi: 10.1016/j.jprot.2018.02.020
PubMed Abstract | CrossRef Full Text | Google Scholar
106. Wiezel GA, Shibao PYT, Cologna CT, Morandi Filho R, Ueira-Vieira C, De Pauw E, et al. In-depth venome of the Brazilian rattlesnake Crotalus durissus terrificus: an integrative approach combining its venom gland transcriptome and venom proteome. J Proteome Res. (2018) 17:3941–58. doi: 10.1021/acs.jproteome.8b00610
PubMed Abstract | CrossRef Full Text | Google Scholar
107. Lamy C, Goodchild SJ, Weatherall KL, Jane DE, Liégeois J-F, Seutin V, et al. Allosteric block of KCa2 channels by apamin. J Biol Chem. (2010) 285:27067–77. doi: 10.1074/jbc.M110.110072
PubMed Abstract | CrossRef Full Text | Google Scholar
108. Adelman JP, Maylie J, Sah P. Small-conductance Ca2+-activated K+ channels: form and function. Annu Rev Physiol. (2012) 74:245–69. doi: 10.1146/annurev-physiol-020911-153336
PubMed Abstract | CrossRef Full Text | Google Scholar
109. Liegeois J, Mercier F, Graulich A, Graulich-Lorge F, Scuvee-Moreau J, Seutin V. Modulation of small conductance calcium-activated potassium (SK) channels: a new challenge in medicinal chemistry. Curr Med Chem. (2003) 10:625–47. doi: 10.2174/0929867033457908
PubMed Abstract | CrossRef Full Text | Google Scholar
110. de Matos Silva LFC, de Paula Ramos ER, Ambiel CR, Correia-de-SáP, Alves-Do-Prado W. Apamin reduces neuromuscular transmission by activating inhibitory muscarinic M(2) receptors on motor nerve terminals. Eur J Pharmacol. (2010) 626:239–43. doi: 10.1016/j.ejphar.2009.09.064
PubMed Abstract | CrossRef Full Text | Google Scholar
111. Alvarez-Fischer D, Noelker C, Vulinović F, Grünewald A, Chevarin C, Klein C, et al. Bee venom and its component apamin as neuroprotective agents in a Parkinson disease mouse model. PLoS ONE. (2013) 8:e61700. doi: 10.1371/journal.pone.0061700
PubMed Abstract | CrossRef Full Text | Google Scholar
112. Messier C, Mourre C, Bontempi B, Sif J, Lazdunski M, Destrade C. Effect of apamin, a toxin that inhibits Ca(2+)-dependent K+ channels, on learning and memory processes. Brain Res. (1991) 551:322–6. doi: 10.1016/0006-8993(91)90950-Z
PubMed Abstract | CrossRef Full Text | Google Scholar
113. Chase TN, Oh-Lee JD. Composition for Treating Parkinson’s Disease (2013). Available online at: https://patents.google.com/patent/WO2013083574A1/en?oq=Thomas%2c+N.C.;+Justin%2c+D.O.L.+Composition+for+Treatins+Parkinsin%E2%80%99s+Disease.+WO2013083574+A1%2c+13+June+2013+ (accessed April 14, 2019).
114. Fox JW. A brief review of the scientific history of several lesser-known snake venom proteins: l-amino acid oxidases, hyaluronidases and phosphodiesterases. Toxicon. (2013) 62:75–82. doi: 10.1016/j.toxicon.2012.09.009
PubMed Abstract | CrossRef Full Text | Google Scholar
115. Boldrini-França J, Cologna CT, Pucca MB, Bordon K de CF, Amorim FG, Anjolette FAP, et al. Minor snake venom proteins: Structure, function and potential applications. Biochim Biophys Acta Gen Subj. (2017) 1861:824–38. doi: 10.1016/j.bbagen.2016.12.022
PubMed Abstract | CrossRef Full Text | Google Scholar
116. Bordon KCF, Perino MG, Giglio JR, Arantes EC. Isolation, enzymatic characterization and antiedematogenic activity of the first reported rattlesnake hyaluronidase from Crotalus durissus terrificus venom. Biochimie. (2012) 94:2740–8. doi: 10.1016/j.biochi.2012.08.014
PubMed Abstract | CrossRef Full Text | Google Scholar
117. Horta CCR, Magalhães B de F, Oliveira-Mendes BBR, do Carmo AO, Duarte CG, Felicori LF, et al. Molecular, immunological, and biological characterization of Tityus serrulatus venom hyaluronidase: new insights into its role in envenomation. PLoS Negl Trop Dis. (2014) 8:e2693. doi: 10.1371/journal.pntd.0002693
PubMed Abstract | CrossRef Full Text | Google Scholar
118. Kreil G. Hyaluronidases–a group of neglected enzymes. Protein Sci. (1995) 4:1666–9. doi: 10.1002/pro.5560040902
PubMed Abstract | CrossRef Full Text | Google Scholar
119. Marković-Housley Z, Miglierini G, Soldatova L, Rizkallah PJ, Müller U, Schirmer T. Crystal structure of hyaluronidase, a major allergen of bee venom. Structure. (2000) 8:1025–35. doi: 10.1016/S0969-2126(00)00511-6
PubMed Abstract | CrossRef Full Text | Google Scholar
120. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase: a biological overview. Life Sci. (2007) 80:1921–43. doi: 10.1016/j.lfs.2007.02.037
PubMed Abstract | CrossRef Full Text | Google Scholar
121. Clinton PM, Kemeny DM, Youlten LJ, Lessof MH. Histamine release from peripheral blood leukocytes with purified bee venom allergens: effect of hyperimmune beekeeper plasma. Int Arch Allergy Appl Immunol. (1989) 89:43–8. doi: 10.1159/000234921
PubMed Abstract | CrossRef Full Text | Google Scholar
122. Habermann E. Bee and wasp venoms. Science. (1972) 177:314–22. doi: 10.1126/science.177.4046.314
PubMed Abstract | CrossRef Full Text | Google Scholar
123. Birr C, Wengert-Müller M. Molecular perspectives of synthetic mast cell-degranulating peptide. In: Eberle AN, Wieland T, Geiger R, editors. Perspectives in Peptide Chemistry. Basel: Karger (1981). p. 372–80.
124. Banks BE, Dempsey CE, Vernon CA, Warner JA, Yamey J. Anti-inflammatory activity of bee venom peptide 401 (mast cell degranulating peptide) and compound 48/80 results from mast cell degranulation in vivo. Br J Pharmacol. (1990) 99:350–4. doi: 10.1111/j.1476-5381.1990.tb14707.x
PubMed Abstract | CrossRef Full Text | Google Scholar
125. Ziai MR, Russek S, Wang H-C, Beer B, Blume AJ. Mast cell degranulating peptide: a multi-functional neurotoxin. J Pharm Pharmacol. (1990) 42:457–61. doi: 10.1111/j.2042-7158.1990.tb06595.x
PubMed Abstract | CrossRef Full Text | Google Scholar
126. Jin A-H, Dutertre S, Dutt M, Lavergne V, Jones A, Lewis RJ, et al. Transcriptomic-proteomic correlation in the predation-evoked venom of the cone snail, Conus imperialis. Mar Drugs. (2019) 17:177. doi: 10.3390/md17030177
PubMed Abstract | CrossRef Full Text | Google Scholar
127. Pucca MB, Amorim FG, Cerni FA, Bordon K de CF, Cardoso IA, Anjolette FAP, et al. Influence of post-starvation extraction time and prey-specific diet in Tityus serrulatus scorpion venom composition and hyaluronidase activity. Toxicon. (2014) 90:326–6. doi: 10.1016/j.toxicon.2014.08.064
PubMed Abstract | CrossRef Full Text | Google Scholar
128. Baracchi D, Turillazzi S. Differences in venom and cuticular peptides in individuals of Apis mellifera (Hymenoptera: Apidae) determined by MALDI-TOF MS. J Insect Physiol. (2010) 56:366–75. doi: 10.1016/j.jinsphys.2009.11.013
PubMed Abstract | CrossRef Full Text | Google Scholar
129. Owen MD, Braidwood JL, Bridges AR. Age dependent changes in histamine content of venom of queen and worker honey bees. J Insect Physiol. (1977) 23:1031–5. doi: 10.1016/0022-1910(77)90131-7
CrossRef Full Text | Google Scholar
130. Bachmayer H, Kreil G, Suchanek G. Synthesis of promelittin and melittin in the venom gland of queen and worker bees: patterns observed during maturation. J Insect Physiol. (1972) 18:1515–21. doi: 10.1016/0022-1910(72)90230-2
CrossRef Full Text | Google Scholar
131. Owen MD. Relationship between age and hyaluronidase activity in the venom of queen and worker honey bees (Apis mellifera L.). Toxicon. (1979) 17:94–8. doi: 10.1016/0041-0101(79)90260-5
PubMed Abstract | CrossRef Full Text | Google Scholar
132. Schumacher MJ, Schmidt JO, Egen NB, Dillon KA. Biochemical variability of venoms from individual European and Africanized honeybees (Apis mellifera). J Allergy Clin Immunol. (1992) 90:59–65. doi: 10.1016/S0091-6749(06)80011-4
PubMed Abstract | CrossRef Full Text | Google Scholar
133. Owen MD. The venom system and venom hyaluronidase of the African honeybee (Apis mellifera Adansonii). Toxicon. (1983) 21:171–4. doi: 10.1016/0041-0101(83)90061-2
PubMed Abstract | CrossRef Full Text | Google Scholar
134. Funari SRC, Zeidler PR, Rocha HC, Sforcin JM. Venom production by Africanized honeybees (Apis mellifera) and Africanized-European hybrids. J Venom Anim Toxins. (2001) 7:190–8. doi: 10.1590/S0104-79302001000200005
CrossRef Full Text | Google Scholar
135. Hoffman DR, Jacobson RS. Allergens in hymenoptera venom XII: how much protein is in a sting? Ann Allergy. (1984) 52:276–8.
PubMed Abstract | Google Scholar
136. Owen MD, Pfaff LA. Melittin synthesis in the venom system of the honey bee (Apis mellifera L.). Toxicon. (1995) 33:1181–8. doi: 10.1016/0041-0101(95)00054-P
PubMed Abstract | CrossRef Full Text | Google Scholar
137. Ferreira Junior RS, Sciani JM, Marques-Porto R, Junior AL, Orsi R de O, Barraviera B, et al. Africanized honey bee (Apis mellifera) venom profiling: seasonal variation of melittin and phospholipase A(2) levels. Toxicon. (2010) 56:355–62. doi: 10.1016/j.toxicon.2010.03.023
PubMed Abstract | CrossRef Full Text | Google Scholar
138. Ediger D, Terzioglu K, Ozturk RT. Venom allergy, risk factors for systemic reactions and the knowledge levels among Turkish beekeepers. Asia Pac. Allergy. (2018) 8:e15. doi: 10.5415/apallergy.2018.8.e15
PubMed Abstract | CrossRef Full Text | Google Scholar
139. Almeida RAM de B, Olivo TET, Mendes RP, Barraviera SRCS, Souza L do R, Martins JG, et al. Africanized honeybee stings: how to treat them. Rev Soc Bras Med Trop. (2011) 44:755–61. doi: 10.1590/S0037-86822011000600020
CrossRef Full Text | Google Scholar
140. Hymenoptera Allergy Committee of the SEAIC, Alfaya Arias T, Soriano Gómis V, Soto Mera T, Vega Castro A, Vega Gutiérrez J, et al. Key issues in hymenoptera venom allergy: an update. J Invest Allergol Clin Immunol. (2017) 27:19–31. doi: 10.18176/jiaci.0123
PubMed Abstract | CrossRef Full Text | Google Scholar
141. Jimenez-Rodriguez TW, Garcia-Neuer M, Alenazy LA, Castells M. Anaphylaxis in the 21st century: phenotypes, endotypes, and biomarkers. J Asthma Allergy. (2018) 11:121–42. doi: 10.2147/JAA.S159411
PubMed Abstract | CrossRef Full Text | Google Scholar
142. Castells MC, Hornick JL, Akin C. Anaphylaxis after hymenoptera sting: is it venom allergy, a clonal disorder, or both? J Allergy Clin Immunol Pract. (2015) 3:350–5. doi: 10.1016/j.jaip.2015.03.015
PubMed Abstract | CrossRef Full Text | Google Scholar
143. Greenhawt M, Akin C. Mastocytosis and allergy. Curr Opin Allergy Clin Immunol. (2007) 7:387–92. doi: 10.1097/ACI.0b013e3282a6443e
PubMed Abstract | CrossRef Full Text | Google Scholar
144. Bonadonna P, Zanotti R, Müller U. Mastocytosis and insect venom allergy. Curr Opin Allergy Clin Immunol. (2010) 10:347–53. doi: 10.1097/ACI.0b013e32833b280c
PubMed Abstract | CrossRef Full Text | Google Scholar
145. Piao X, Bernstein A. A point mutation in the catalytic domain of c-kit induces growth factor independence, tumorigenicity, and differentiation of mast cells. Blood. (1996) 87:3117–23.
PubMed Abstract | Google Scholar
146. Dart RC. Medical Toxicology. Philadelphia, PA: Lippincott Williams and Wilkins (2004).
147. Nisahan B, Selvaratnam G, Kumanan T. Myocardial injury following multiple bee stings. Trop Doct. (2014) 44:233–4. doi: 10.1177/0049475514525606
PubMed Abstract | CrossRef Full Text | Google Scholar
148. James ES, Walker WG. ACTH in wasp stings. Med Assoc J. (1952) 67:50–1.
PubMed Abstract | Google Scholar
149. Ross AT. Peripheral neuritis: allergy to honeybee stings. J Allergy. (1939) 10:382–4. doi: 10.1016/S0021-8707(39)90154-1
CrossRef Full Text | Google Scholar
150. Marks HG, Augustyn P, Allen RJ. Fisher’s syndrome in children. Pediatrics. (1977) 60:726–9.
PubMed Abstract | Google Scholar
151. Bachman DS, Paulson GW, Mendell JR. Acute inflammatory polyradiculoneuropathy following hymenoptera stings. JAMA. (1982) 247:1443–5. doi: 10.1001/jama.247.10.1443
PubMed Abstract | CrossRef Full Text | Google Scholar
152. Maltzman JS, Lee AG, Miller NR. Optic neuropathy occurring after bee and wasp sting. Ophthalmology. (2000) 107:193–5. doi: 10.1016/S0161-6420(99)00020-2
PubMed Abstract | CrossRef Full Text | Google Scholar
153. Truskinovsky AM, Dick JD, Hutchins GM. Fatal infection after a bee sting. Clin Infect Dis. (2001) 32:E36–8. doi: 10.1086/318451
PubMed Abstract | CrossRef Full Text | Google Scholar
154. Venkataramanappa SK, Gowda A, Raju S, Harihar V. An unusual case of bilateral empyema associated with bee sting. Case Rep Med. (2014) 2014:985720. doi: 10.1155/2014/985720
PubMed Abstract | CrossRef Full Text | Google Scholar
155. Kaya A, Okur M. Bee sting in mother and urticarial rash in her baby. Indian Pediatr. (2012) 49:499.
PubMed Abstract | Google Scholar
156. Przybilla B, Ruëff F. Insect Stings. Minich: Deutsches Aerzteblatt (2012).
157. Gordon RM. Reactions produced by arthropods. BMJ. (1950) 2:316–8. doi: 10.1136/bmj.2.4674.316
PubMed Abstract | CrossRef Full Text | Google Scholar
158. Kragballe K. Topical corticosteroids: mechanisms of action. Acta Derm Venereol Suppl. (1989) 151:7–10.
PubMed Abstract | Google Scholar
159. Sherman RA. What physicians should know about Africanized honeybees. West J Med. (1995) 163:541–6.
PubMed Abstract | Google Scholar
160. da Silva GB, Vasconcelos AG, Rocha AMT, de Vasconcelos VR, de Barros J, Fujishima JS, et al. Acute kidney injury complicating bee stings–a review. Rev Inst Med Trop São Paulo. (2017) 59:e25. doi: 10.1590/s1678-9946201759025
CrossRef Full Text | Google Scholar
161. Muraro A, Roberts G, Worm M, Bilò MB, Brockow K, Rivas MF, et al. Anaphylaxis: guidelines from the European Academy of Allergy and Clinical Immunology. Allergy. (2014) 69:1026–45. doi: 10.1111/all.12437
PubMed Abstract | CrossRef Full Text | Google Scholar
162. Simons FER, Ebisawa M, Sanchez-Borges M, Thong BY, Worm M, Tanno LK, et al. 2015 update of the evidence base: World Allergy Organization anaphylaxis guidelines. World Allergy Organ J. (2015) 8:32. doi: 10.1186/s40413-015-0080-1
PubMed Abstract | CrossRef Full Text | Google Scholar
163. Dudley LS, Mansour MI, Merlin MA. Epinephrine for anaphylaxis: underutilized and unavailable. West J Emerg Med. (2015) 16:385–7. doi: 10.5811/westjem.2015.3.25337
PubMed Abstract | CrossRef Full Text | Google Scholar
164. Campbell RL, Manivannan V, Hartz MF, Sadosty AT. Epinephrine auto-injector pandemic. Pediatr Emerg Care. (2012) 28:938–42. doi: 10.1097/PEC.0b013e318267f689
PubMed Abstract | CrossRef Full Text | Google Scholar
165. Brown AF. Therapeutic controversies in the management of acute anaphylaxis. Emerg Med J. (1998) 15:89–95. doi: 10.1136/emj.15.2.89
PubMed Abstract | CrossRef Full Text | Google Scholar
166. Lieberman P, Nicklas RA, Randolph C, Oppenheimer J, Bernstein D, Bernstein J, et al. Anaphylaxis—a practice parameter update 2015. Annal Allergy Asthma Immunol. (2015) 115:341–84. doi: 10.1016/j.anai.2015.07.019
CrossRef Full Text | Google Scholar
167. Simons FER, Ardusso LRF, Bilò MB, El-Gamal YM, Ledford DK, Ring J, et al. World Allergy Organization anaphylaxis guidelines: summary. J Allergy Clin Immunol. (2011) 127:587–93.e22. doi: 10.1016/j.jaci.2011.01.038
PubMed Abstract | CrossRef Full Text | Google Scholar
168. Incorvaia C, Frati F, Dell’Albani I, Robino A, Cattaneo E, Mauro M, et al. Safety of hymenoptera venom immunotherapy: a systematic review. Expert Opin Pharmacother. (2011) 12:2527–32. doi: 10.1517/14656566.2011.616494
PubMed Abstract | CrossRef Full Text | Google Scholar
169. Sturm GJ, Varga E-M, Roberts G, Mosbech H, Bilò MB, Akdis CA, et al. EAACI guidelines on allergen immunotherapy: hymenoptera venom allergy. Allergy. (2018) 73:744–64. doi: 10.1111/all.13262
PubMed Abstract | CrossRef Full Text | Google Scholar
170. Głobińska A, Boonpiyathad T, Satitsuksanoa P, Kleuskens M, van de Veen W, Sokolowska M, et al. Mechanisms of allergen-specific immunotherapy: diverse mechanisms of immune tolerance to allergens. Ann Allergy Asthma Immunol. (2018) 121:306–12. doi: 10.1016/j.anai.2018.06.026
PubMed Abstract | CrossRef Full Text | Google Scholar
171. Boyle RJ, Elremeli M, Hockenhull J, Cherry MG, Bulsara MK, Daniels M, et al. Venom immunotherapy for preventing allergic reactions to insect stings. Coch Datab Syst Rev. (2012) 10:CD008838. doi: 10.1002/14651858.CD008838.pub2
PubMed Abstract | CrossRef Full Text | Google Scholar
172. Mitchell A. Africanized killer bees A case study. Crit Care Nurse. (2006) 26:23–31.
PubMed Abstract | Google Scholar
173. Tunget CL, Clark RF. Invasion of the “killer” bees. Separating fact from fiction. Postgrad Med. (1993) 94:92–4. doi: 10.1080/00325481.1993.11945694
PubMed Abstract | CrossRef Full Text | Google Scholar
174. Bresolin NL, Carvalho FC, Goes JC, Fernandes V, Barotto AM. Acute renal failure following massive attack by Africanized bee stings. Pediatr Nephrol. (2002) 17:625–7. doi: 10.1007/s00467-002-0888-0
PubMed Abstract | CrossRef Full Text | Google Scholar
175. Abbas AK, Lichtman AH, Pillai S. Basic Immunology: Functions and Disorders of the Immune System. 5th ed. St. Louis, MO: Elsevier (2016).
176. Schumacher MJ, Egen NB, Tanner D. Neutralization of bee venom lethality by immune serum antibodies. Am J Trop Med Hyg. (1996) 55:197–201. doi: 10.4269/ajtmh.1996.55.197
PubMed Abstract | CrossRef Full Text | Google Scholar
177. King TP, Sobotka AK, Kochoumian L, Lichtenstein LM. Allergens of honey bee venom. Arch Biochem Biophys. (1976) 172:661–71. doi: 10.1016/0003-9861(76)90121-1
PubMed Abstract | CrossRef Full Text | Google Scholar
178. Terra RMS. Análise Conformacional da Melitina por Dinâmica Molecular e Caracterização dos Efeitos do Peptídeo na Função Plaquetária. Universidade do Rio Grande do Sul, Porto Alegre, Brazil (2006). Available online at: https://lume.ufrgs.br/handle/10183/10943
179. Jones RG, Bhogal G, Corteling RL, Landon J. A novel Fab-based antivenom for the treatment of mass bee attacks. Am J Trop Med Hyg. (1999) 61:361–6. doi: 10.4269/ajtmh.1999.61.361
PubMed Abstract | CrossRef Full Text | Google Scholar
180. Santos KS, Stephano MA, Marcelino JR, Ferreira VMR, Rocha T, Caricati C, et al. Production of the first effective hyperimmune equine serum antivenom against Africanized bees. PLoS ONE. (2013) 8:e79971. doi: 10.1371/journal.pone.0079971
PubMed Abstract | CrossRef Full Text | Google Scholar
181. Barbosa AN, Boyer L, Chippaux J-P, Medolago NB, Caramori CA, Paixão AG, et al. A clinical trial protocol to treat massive Africanized honeybee (Apis mellifera) attack with a new apilic antivenom. J Venom Anim Toxins Incl Trop Dis. (2017) 23:14. doi: 10.1186/s40409-017-0106-y
PubMed Abstract | CrossRef Full Text | Google Scholar
182. Laustsen AH, Gutiérrez JM, Knudsen C, Johansen KH, Bermúdez-Méndez E, Cerni FA, et al. Pros and cons of different therapeutic antibody formats for recombinant antivenom development. Toxicon. (2018) 146:151–75. doi: 10.1016/j.toxicon.2018.03.004
PubMed Abstract | CrossRef Full Text | Google Scholar
183. Pucca MB, Cerni FA, Janke R, Bermúdez-Méndez E, Ledsgaard L, Barbosa JE, et al. History of envenoming therapy and current perspectives. Front Immunol. (2019) 10:1598. doi: 10.3389/fimmu.2019.01598
PubMed Abstract | CrossRef Full Text | Google Scholar
184. LoVecchio F, Klemens J, Roundy EB, Klemens A. Serum sickness following administration of Antivenin (Crotalidae) Polyvalent in 181 cases of presumed rattlesnake envenomation. Wilderness Environ Med. (2003) 14:220–1. doi: 10.1580/1080-6032(2003)14[220:SSFAOA]2.0.CO;2
PubMed Abstract | CrossRef Full Text | Google Scholar
185. León G, Herrera M, Segura Á, Villalta M, Vargas M, Gutiérrez JM. Pathogenic mechanisms underlying adverse reactions induced by intravenous administration of snake antivenoms. Toxicon. (2013) 76:63–76. doi: 10.1016/j.toxicon.2013.09.010
PubMed Abstract | CrossRef Full Text | Google Scholar
186. Laustsen AH, Karatt-Vellatt A, Masters EW, Arias AS, Pus U, Knudsen C, et al. In vivo neutralization of dendrotoxin-mediated neurotoxicity of black mamba venom by oligoclonal human IgG antibodies. Nat Commun. (2018) 9:3928. doi: 10.1038/s41467-018-06086-4
CrossRef Full Text | Google Scholar
187. Pucca MB, Cerni FA, Peigneur S, Arantes EC, Tytgat J, Barbosa JE. Serrumab: a novel human single chain-fragment antibody with multiple scorpion toxin-neutralizing capacities. J Immunotoxicol. (2014) 11:133–40. doi: 10.3109/1547691X.2013.809175
PubMed Abstract | CrossRef Full Text | Google Scholar
188. Silva LC, Pucca MB, Pessenda G, Campos LB, Martinez EZ, Cerni FA, et al. Discovery of human scFvs that cross-neutralize the toxic effects of B. jararacussu and C. d. terrificus venoms. Acta Tropica. (2018) 177:66–73. doi: 10.1016/j.actatropica.2017.09.001
PubMed Abstract | CrossRef Full Text | Google Scholar
189. Laustsen AH, Johansen KH, Engmark M, Andersen MR. Recombinant snakebite antivenoms: a cost-competitive solution to a neglected tropical disease? PLoS Negl Trop Dis. (2017) 11:e0005361. doi: 10.1371/journal.pntd.0005361
PubMed Abstract | CrossRef Full Text | Google Scholar
190. Funayama JC, Pucca MB, Roncolato EC, Bertolini TB, Campos LB, Barbosa JE. Production of human antibody fragments binding to melittin and phospholipase A2 in Africanised bee venom: minimising venom toxicity. Basic Clin Pharmacol Toxicol. (2012) 110:290–7. doi: 10.1111/j.1742-7843.2011.00821.x
PubMed Abstract | CrossRef Full Text | Google Scholar
191. Pessenda G, Silva LC, Campos LB, Pacello EM, Pucca MB, Martinez EZ, et al. Human scFv antibodies (Afribumabs) against Africanized bee venom: advances in melittin recognition. Toxicon. (2016) 112:59–67. doi: 10.1016/j.toxicon.2016.01.062
PubMed Abstract | CrossRef Full Text | Google Scholar
192. Yonamine CM, Costa H, Silva J a. A,, Muramoto E, Rogero JR, Troncone LRP. Biodistribution studies of bee venom and spider toxin using radiotracers. J Venom Anim Toxins Incl Trop Dis. (2005) 11:39–50. doi: 10.1590/S1678-91992005000100006
CrossRef Full Text | Google Scholar
193. Jenkins T, Fryer T, Dehli R, Jürgensen J, Fuglsang-Madsen A, Føns S, et al. Toxin neutralization using alternative binding proteins. Toxins. (2019) 11:53. doi: 10.3390/toxins11010053
PubMed Abstract | CrossRef Full Text | Google Scholar
194. Laustsen AH. Guiding recombinant antivenom development by omics technologies. N Biotechnol. (2018) 45:19–27. doi: 10.1016/j.nbt.2017.05.005
PubMed Abstract | CrossRef Full Text | Google Scholar
Zdroj:
https://www.frontiersin.org/articles/10.3389/fimmu.2019.02090/full#B1

